Timidin
| Timidin | |||

| |||
| |||
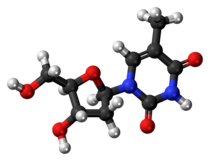
| IUPAC-név | Timidin | ||
| Szabályos név | 1-[(2R,4S,5R)-4-hidroxi-5-(hidroximetil)oxolán-2-il]-5-metilpirimidin-2,4(1H,3H)-dion | ||
| Más nevek | dezoxitimidin, Td, dT, 1-[(2R,4S,5R)-4-hidroxi-5-(hidroximetil)tetrahidrofur-2-il]-5-metil-1,3-dihidropirimidin-2,4-dion | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 50-89-5 | ||
| PubChem | 1134 | ||
| ChemSpider | 5585 | ||
| DrugBank | DB04485 | ||
| MeSH | Deoxythymidine | ||
| |||
| |||
| InChIKey | IQFYYKKMVGJFEH-XLPZGREQSA-N | ||
| UNII | VC2W18DGKR | ||
| ChEMBL | 52609 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C10H14N2O5 | ||
| Moláris tömeg | 242,23 g/mol | ||
| Olvadáspont | 185 °C | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A timidin (jele dT vagy dThd, más néven dezoxitimidin, dezoxiriboziltimin vagy timin dezoxiribozid) pirimidin-dezoxinukleozid. Ez felel meg a DNS T nukleozidjának, mely a dezoxiadenozinnal van párban a kétszálú DNS-ben. A sejtek G1/korai S fázisba való szinkronizálására használatos. A „dezoxi-” előtagot gyakran elhagyják, mivel nincs timinnukleotid-prekurzor az RNS-szintézisben.
A timidint használata növekedése előtt, melyet az azidotimidin antiretrovirális szer termelése okozott nagy részt heringspermából termelték.[1] A timidin a DNS mellett a tRNS T-ciklusában is előfordul.
Szerkezet, tulajdonságok
[szerkesztés]A dezoxitimidin dezoxiribózból (pentóz) áll, mely a timinhez, egy pirimidin-nukleobázishoz csatlakozik.
1, 2 vagy 3 foszfátcsoporttal foszforilálható, ezek terméke a dezoxitimidin-mono-, -di-, illetve a -trifoszfát (dTMP, dTDP, illetve dTTP).
Szilárd halmazállapotban kis fehér kristályokat alkot vagy por. Moláris tömege 242.229 g/mol, olvadáspontja 185 °C. Normál körülmények közt nagyon stabil.
A dezoxitimidin nem mérgező, és a DNS négy nukleozidjának egyikeként természetesen előforduló vegyület, mely minden élőlényben és DNS-vírusban megtalálható. Az RNS-ben a timidin helyén uridin (ribózhoz csatlakozó uracil) van. Az uracil kémiailag hasonlít a timinre, melynek további neve 5-metiluracil is. Mivel a timinnukleotidok a DNS prekurzorai, de nem az RNS-éi, a „dezoxi-” előtag gyakran kimarad, vagyis a dezoxitimidin gyakran timidinként szerepel.
A timidin a kémiai teratogének listáján szerepel.[2]
Származékok
[szerkesztés]- A jód-dezoxiuridin radioaktivitásra érzékenyít, és növeli az ionizáló sugárzás okozta DNS-károsodást.
- Az azidotimidin (AZT) a HIV-fertőzés kezelésében használatos, mivel reverztranszkriptáz-gátló, akadályozva a HIV replikációs ciklusát.
- A radioaktív anyaggal, például tríciummal (3H-TdR) jelölt timidin (TdR) gyakran használatos sejtproliferációs assay-kben. A timidin az osztódó sejtekbe kerül, ennek mértéke, mely szcintillációs számlálóval mérhető, egyenesen arányos a sejtosztódás mértékével. Így például a limfocita-proliferáció is mérhető limfoproliferatív rendellenességek diagnózisához.
- A bróm-dezoxiuridin gyakran használatos osztódó sejtek észlelésére élő szövetekben.
- Az 5-etinil-2’-dezoxiuridin szintén bekerül az osztódó sejtek DNS-ébe, és sejttenyészetben vagy élő szövetekben lévő DNS-szintézis mérésére használható. Klikk-kémia használatával fluoreszcens azid kötésével szemléltethető, ami kevésbé erős, mint a BrdU antitestek epitópjának kimutatása.
- Az edoxudin vírusellenes szer.
- A telbivudin (β-l-2’-dezoxitimidin, LdT) a timidin módosítatlan l-enantiomerje krónikus hepatitis B-re.[3]
A timidinfelesleg és a mutációk kapcsolata
[szerkesztés]A T4 bakteriofág növekedése során a megnövekedő timidinmennyiség növeli a mutációk számát.[4][5] A timidinhiány is növeli a mutáció mértékét.[4] A Saccharomyces cerevisiae timidin-auxotrófját is különböző timidinszintek mellett vizsgálták kutatók.[6] A sok timidin mutagén és rekombinogén volt, a kevés bár rekombinogén volt, de kevésbé mutagén.
Jegyzetek
[szerkesztés]- ↑ „Enzymatic Production of 5-Methyluridine from Purine Nucleosides and Thymine by Erwinia carotovora AJ-2992”, Kiadó: Agricultural and Biological Chemistry.
- ↑ Az ismert vagy feltételezett teratogének listája nagyrészt innen: N. Irving Sax, Richard J. Lewis. Dangerous Properties of Industrial Materials, 7.
- ↑ (2008) „LdT (telbivudine) as a potent and specific nucleoside analogue (Tyzeka™, Sebivo™) for the treatment of chronic hepatitis B”. Collection Symposium Series, 244–248. o. DOI:10.1135/css200810244.
- ↑ a b Bernstein C, Bernstein H, Mufti S, Strom B (1972. október). „Stimulation of mutation in phage T 4 by lesions in gene 32 and by thymidine imbalance”. Mutat Res 16 (2), 113–119. o. DOI:10.1016/0027-5107(72)90171-6. PMID 4561494.
- ↑ DeVries JK, Wallace SS (1982). „Reversion of bacteriophage T4rII mutants by high levels of pyrimidine deoxyribonucleosides”. Mol Gen Genet 186 (1), 101–105. o. DOI:10.1007/BF00422919. PMID 7050620.
- ↑ Eckardt F, Kunz BA, Haynes RH. Variation of mutation and recombination frequencies over a range of thymidylate concentrations in a diploid thymidylate auxotroph (1983. szeptember). „Curr Genet” 7 (5), 399–402. o. DOI:10.1007/BF00445881. PMID 24173422.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Thymidine című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
