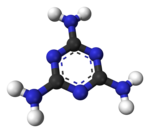
Melamin
| Melamin | |||
 |
| ||
| IUPAC-név | 1,3,5-triazin-2,4,6-triamin | ||
| Más nevek | 2,4,6-triamino-sz-triazin[Jegyzet 1] cianuramid cianurotriamid cianurotriamin triaminotriazin | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 108-78-1 | ||
| PubChem | 7955 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C3H6N6 | ||
| Moláris tömeg | 126,12 g/mol | ||
| Megjelenés | fehér, szilárd, kristályos | ||
| Sűrűség | 1574 kg/m³ | ||
| Olvadáspont | 350 °C | ||
| Forráspont | szublimál | ||
| Oldhatóság (vízben) | 3,1 g/dm³ (20 °C) | ||
| Veszélyek | |||
| EU osztályozás | nincsenek veszélyességi szimbólumok[1] | ||
| R mondatok | (nincs)[1] | ||
| S mondatok | (nincs)[1] | ||
| LD50 | 3160 mg/kg (patkány, szájon át)[1] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A melamin egy nitrogéntartalmú, heterociklusos, aromás szerves vegyület. Elsősorban a műanyagiparban alkalmazzák.
A vegyületet Justus von Liebig nevezte el a melam[2] nevű vegyületről, az amin végződéssel kiegészítve. A melam név a görög melasz (μέλας = fekete, sötét színű) szóból származik.[3]
Előállítása
[szerkesztés]Előállítása ipari méretekben kalcium-ciánamidból történik. A kalcium-ciánamidból szénsavval vagy kénsavval ciánamidot szabadítanak fel, ezt alacsony hőmérsékleten való bepárlással nyerik ki. A ciánamidot enyhén lúgos oldatban (pH = 8-12), 50-80 °C-on dimerizálják, így diciándiamid képződik (képleteket lásd lejjebb). A diciándiamidot metanolos ammóniaoldatban, 160 °C-on, zárt térben hevítve egy tautomer vegyületen keresztül egy gyűrűs, trimer termék, a melamin képződik.

Felhasználása
[szerkesztés]A műanyaggyártásban
[szerkesztés]
A műanyagiparban a karbamidhoz hasonló tulajdonságai miatt formaldehidgyanták készítésére alkalmazzák. A gyártási folyamat során a melamint formaldehiddel reagáltatják.[4] Az így nyert formaldehidgyanták hálózatos szerkezetű, hőre keményedő műanyagok. A bennük lévő szabad aminocsoportok (-NH2) könnyen reagálnak más vegyületek funkciós csoportjaival, pl. karboxil- (-COOH), hidroxil- -(OH) és amidcsoportokkal (-CONH-), így a melaminos formaldehidgyanta könnyen megkötődik más műanyagok felületén.[5] E tulajdonságai miatt különféle műanyagok (pl. akrilátok, poliészterek, epoxigyanták) festésére használják.[5]
Rovarölőszerként
[szerkesztés]A melamin ciromazin nevű származékát rovarölőszerként használják, mivel akadályozza a rovarok vedlését és bebábozódását.[6] A ciromazin melaminként beépül a növényekbe, így bekerül a táplálékláncba is.[7] Az emberben nagy mennyiségben vesekövességet okoz, hosszú távú hatásai egyelőre ismeretlenek.[7]
Jegyzetek
[szerkesztés]- ↑ A képletben szereplő sz jelölés a molekula szimmetrikusságára utal.
Források
[szerkesztés]- Bruckner Győző: Szerves kémia I. (Tankönyvkiadó, Budapest, 1973)
- Dr. Lempert Károly: Szerves kémia (Műszaki Könyvkiadó, Budapest, 1976, ISBN 963-10-1191-7)
További információk
[szerkesztés]- ↑ a b c d A melamin vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2011. január 20. (JavaScript szükséges) (angolul)
- ↑ Melam (ChemSpider)
- ↑ Fülöp József: Rövid kémiai értelmező és etimológiai szótár. Celldömölk: Pauz–Westermann Könyvkiadó Kft. 1998. 96. o. ISBN 963 8334 96 7
- ↑ Melamin és formaldehid reakciója Archiválva 2008. október 1-i dátummal a Wayback Machine-ben, majd a termék kondenzációja (műanyag képződése) Archiválva 2008. október 1-i dátummal a Wayback Machine-ben (szerző: Guomin Byan, Clarkson University Archiválva 2008. szeptember 15-i dátummal a Wayback Machine-ben)
- ↑ a b Thermosetting Resins Archiválva 2008. október 6-i dátummal a Wayback Machine-ben (The Laboratory of Microcantilever Technology, Louisiana Tech University) Archiválva 2008. október 6-i dátummal a Wayback Machine-ben
- ↑ Frederick M. Fishel: Pesticide Toxicity Profile: Triazine Pesticides (Electronic Data Information Source, University of Florida)
- ↑ a b Melamine in pesticides, human food chain - experts (szerző: Tan Ee Lyn, Reuters Egyesült Királyság Archiválva 2009. május 2-i dátummal a Wayback Machine-ben)
