Trifluortoluol
| Trifluortoluol | |||
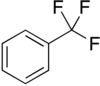 |

| ||
| Más nevek | Benzotrifluorid α,α,α-Trifluortoluol | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 98-08-8 | ||
| PubChem | 7368 | ||
| ChemSpider | 7090 | ||
| EINECS-szám | 202-635-0 | ||
| |||
| |||
| UNII | 49R6421K89 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C6H5CF3 | ||
| Moláris tömeg | 146,11 g/mol | ||
| Megjelenés | színtelen folyadék | ||
| Szag | aromás | ||
| Sűrűség | 1,19 g/mL (20 °C-on) | ||
| Olvadáspont | -29,05 °C | ||
| Forráspont | 103,46 °C | ||
| Oldhatóság (vízben) | <0,1 g/100 ml (21 °C-on) | ||
| Oldhatóság | oldódik éterben, benzolban, etanolban, acetonban, korlátlanul elegyedik n-heptánnal, CCl4-dal | ||
| Törésmutató (nD) | 1,41486 (13 °C) | ||
| Veszélyek | |||
| NFPA 704 | |||
| Lobbanáspont | 12 °C | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A trifluortoluol szerves vegyület, a toluol fluorozott származéka, képlete C6H5CF3. Színtelen folyadék, szerves kémiai szintézisek speciális oldószereként használják, valamint peszticidek és gyógyszerhatóanyagok előállításának köztiterméke.[1]
Előállítása
[szerkesztés]Kisléptékű laboratóriumi előállítása aril-halogenid és trifluor-jódmetán rézkatalizátor jelenlétében történő kapcsolásával történhet:[2]
- PhX + CF3I → PhCF3 (X = I, Br)
Iparilag benzotriklorid és hidrogén-fluorid nagynyomású reaktorban történő reagáltatásával gyártják.[3]
- PhCCl3 + 3 HF → PhCF3 + 3 HCl
Felhasználása
[szerkesztés]A diklórmetán kevéssé mérgező kiváltója
[szerkesztés]Ogawa és Curran szerint a szokásos acilezési, tozilezési és szililezési reakciókban a a trifluortoluol hasonlít a diklórmetánhoz.[4] A diklórmetán és trifluortoluol dielektromos állandója rendre 9,04, illetve 9,18, ami hasonló szolvatációs tulajdonságokat jelez. Dipólusmomentumuk már kevésbé egyezik, ezek rendre 1,89, illetve 2,86 D. A diklórmetán kiváltása előnyös, ha a körülmények magasabb forráspontú oldószert igényelnek, mivel a trifluortoluol forráspontja 62 °C-kal magasabb, mint a diklórmetáné (40 °C).
A trifluortoluol hasznos oldószer az enyhe Lewis-savak által katalizált reakciókban, mint például a Friedel–Crafts-reakciók. Bár a leggyakrabban használt alumínium-klorid-katalizátor szobahőmérsékleten reakcióba lép a trifluortoluollal, a cink-klorid azonban nem.
Szintézis köztitermék
[szerkesztés]További, feltehetően fontosabb felhasználása más vegyületek szintézise. Egyik származéka, a 3-aminobenzotrifluorid a fluometuron nevű herbicid szintézisének prekurzora.[3] Előbbit a trifluortoluol nitrálásával, majd redukciójával nyerik (ennek eredménye meta-H2NC6H4CF3), majd ebből az aromás aminből állítják elő a karbamidszármazék herbicidet.
A flumetramid (6-[4-(trifluormetil)fenil]morfolin-3-on) nevű vázizomrelaxánst is trifluortoluolból állítják elő.[1]
Analitika
[szerkesztés]A 19F NMR-spektrumában egyetlen szingulett jel található -63,2 ppm-nél.[5]
Jegyzetek
[szerkesztés]- ↑ a b Banks, R.E. Organofluorine Chemicals and their Industrial Applications, Ellis Horwood LTD, Chichester, 1979.
- ↑ Ogawa, Akiya; Tsuchii, Kaname "α,α,α-Trifluorotoluene" in Encyclopedia of Reagents for Organic Synthesis 2005, John Wiley and Sons. doi:10.1002/047084289X.rn00653
- ↑ a b Siegemund, Günter "Aromatic Compounds with Fluorinated Side-Chains" in Ullmann’s Encyclopedia of Industrial Chemistry 2005, Wiley-VCH. doi:10.1002/14356007.a11_349.
- ↑ (1997) „Benzotrifluoride: A Useful Alternative Solvent for Organic Reactions Currently Conducted in Dichloromethane and Related Solvents”. Journal of Organic Chemistry 62 (3), 450–451. o. DOI:10.1021/jo9620324.
- ↑ (2010. február 3.) „Mechanistic Duality in Palladium-Catalyzed Cross-Coupling Reactions of Aryldimethylsilanolates. Intermediacy of an 8-Si-4 Arylpalladium(II) Silanolate (Supplementary Material, referenced as PhCF3)”. Journal of the American Chemical Society 132 (4), 1243–1245. o. DOI:10.1021/ja907049y. PMID 20058920. PMC 2812642.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Trifluorotoluene című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.

