Monoklonális antitest
A monoklonális antitestek olyan antitestek (ellenanyagok) amelyeket egyetlen fehérvérsejtből kiinduló, klónozott sejtvonal termel, így szerkezetileg egységesek és egy bizonyos antigén egy bizonyos epitopjához kötődnek (szemben a poliklonális antitestekkel, amelyeket több sejt állít elő és a célmolekula több pontjához kötődnek változó hatékonysággal). Molekuláris biológiai módszerekkel, két ellenanyag-molekula összekötésével olyan monoklonális antitestek is előállíthatók, amelyek két epitóphoz is kötődnek.
Monoklonális antitestek szinte minden nagyobb molekula ellen előállíthatóak és specifikus kötődésük miatt a kutatásban, az orvostudományban, az iparban egyaránt széleskörűen használják őket a célmolekula detektálására vagy tisztítására. A gyógyításban súlyos betegségek diagnosztizálására és terápiájára is felhasználhatóak.[3] Újabban a Covid19 tüneteinek egyhítésére alkalmazzák.[4]
Kutatástörténet
[szerkesztés]A Nobel-díjas Paul Ehrlich már az 1900-as években felvetette az immunológiai "varázslövedék" (Zauberkugel) lehetőségét: egy olyan vegyületet, amely specifikusan kötődik a kórokozóhoz és a hozzákötött toxinnal el is pusztítja azt. Ennek megvalósításához azonban akkor még hiányzott a megfelelő technológiai háttér.
Az 1970-es évekre felfedezték, hogy az antitesteket termelő B-limfociták tumora (mielóma multiplex) során létrejönnek olyan, kontrollálatlanul növekvő sejtvonalak, amelyek egy bizonyos antitest-molekulát állítanak elő. Ezeket az abnormális antitesteket (többnyire a teljes fehérje csak egy részét, pl. a könnyű láncot tartalmazták) előszeretettel használták az ellenanyagok szerkezetének kutatásában, de ekkor még nem volt lehetséges egy konkrét antigén ellen termeltetni azonos antitesteket.[5]:324 1973-ban az amerikai Jerrold Schwaber először állított elő ún. hibridómákat: emberi limfocitákat egyesítettek egér mielómás tumorsejtekkel.[6] Két évvel később a német Georges Köhler és az argentin César Milstein olyan hibridómákat állított elő, amelyek egy adott antigén ellen termeltek ellenanyagot és immortalizáltak voltak (a végtelenségig képesek voltak osztódni).[7] Ők ketten (Niels Kaj Jernével megosztva) a munkájukért 1984-ben elnyerték az orvostudományi Nobel-díjat.[7]
1988-ban Gregory Winternek és csapatának sikerült "humanizálnia" (az emberéhez hasonlóvá tennie) a monklonális antitesteket,[8] megszüntetve így az immunrekaciót, amely egyes betegekben jelentkezett az antitestek beadása után. Az 1990-es években megkezdődtek a kísérletek a monoklonális antitestek terápiás alkalmazására. 2018-ban James P. Allison és Hondzso Taszuku orvosi Nobel-díjban részesült új tumerterápiás módszerükért, melyben monklonális antitestekkel akadályozták meg az immunválasz gátlását.[9]
Előállítása
[szerkesztés]

A hibridómák előállítása
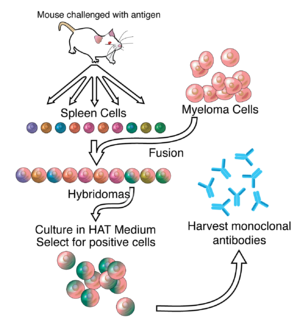
[szerkesztés]A monoklonális antitestek termelésében a legnagyobb feladat a megfelelő hibridómák előállítása, ezen belül azoknak a hibrid sejteknek az azonosítása, amelyek a szükséges ellenanyagot termelik.[7] Erre a célra általában nyúlsejteket használnak. A lép sejtjeit összekeverik a mielómasejtekkel, majd polietilén-glikol segítségével fuzionáltatják az egymás melletti sejtek plazmamembránját.[10] A fúzió hatásfoka eléggé alacsony, ezért olyan szelektív tenyésztőközeget használnak, amelyben csak a hibrid sejtek képesek osztódni hosszabb távon. A folyamatban alkalmazott mielómasejtekben elrontották a hipoxantin-guanin foszforiboziltranszferáz (HGPRT) enzimet, amely a nukleinsavak újrahasznosításához szükséges. Az enzim hiánya önmagában nem okoz gondot, de ha a nukleinsavak újonnan való szintézisét is blokkolják (pl. aminopterinnel), a sejt képtelen osztódni.
Mivel a szelektív tápközeg aminopterint tartalmaz, a nem fuzionáló mielómasejtek nem tudnak szaporodni, a nem fuzionáló lépsejtek pedig néhány osztódás után természetes módon elpusztulnak, így hosszabb távon csak a hibridómák maradnak életben, amelyek a mielóma felük miatt immortalizáltak (mint a tumorsejtek), plazmasejt felük után pedig tartalmaznak HGPRT enzimet.
A fenti sejtkeveréket annyira felhígítják, hogy a tápközeget szétosztva a további tenyésztést egy-egy sejtből tudják folytatni, vagyis klónozzák őket. Ezután valamilyen immunoassay teszttel (ELISA, antigén microarray, dot blot) megvizsgálják az egyes sejtklónok által termelt ellenanyagok kötődési képességét a kívánt antigénhez és a legbiztosabb, legstabilabb klónt viszik tovább az ipari szintű termelésbe.
Megfelelő tápközegben a hibridómák a végtelenségig tenyészthetők. Esetenként egér hashártyaüregébe injektálják, ahol a sejtek tumorokat alkotnak, amely ellenanyagokban gazdag folyadékot választ ki (utóbbi módszert etikai okokból csak akkor használják, ha más alternatíva nem áll rendelkezésre).[11]
A hagyományos hibrima-nódszer mellett új technológiákkal is kísérleteznek;[12] ezekben többnyire az ellenanyag könnyű és nehéz láncát viszik be rekombináns módszerekkel baktériumokba vagy emlőssejtekbe, amelyeket hatékonyabban lehet tenyészteni és a nyúlon kívül másfajta sejteket is használhatnak.
A megtermelt ellenanyagot a sejttenyészet felülúszójából vagy a hashártyafolyadékból nyerik ki különböző tisztítási lépésekkel (szűrés, ioncserélő kromatográfia vagy affinitás-kromatográfia).
A monoklonális ellenanyagot molekuláris biológiai módszerekkel (klónozás, CRISPR/Cas9, fág- vagy élesztő-display)tovább lehet fejleszteni.[13] Az ellenanyag génjének kissé módosított változatait beviszik egy vírus vagy élesztőgomba genomjába, majd a megfelelő szűrőmódszerekkel kiválasztják azokat a verziókat, amelyek a legjobban kötnek, legstabilabbak, leghatékonyabbak a terápiában, stb.[14] The phage antibody libraries are a variant of phage antigen libraries.[15][16] A vírusok és az élesztőgombák alkalmasabbak is az ipari léptékű, fermentációs tartályokban történő termelésre, mint az érzékenyebb emlőssejtek.
Kiméra ellenanyagok
[szerkesztés]A terápiában felhasznált monoklonális ellenanyagokat korábban állatokban (egérben) állították elő, és gyakran immunválaszt lépett fel az idegen eredetű antitestekkel szemben. A probléma megoldására kiméra-antitesteket hoztak létre ("humanizálták" az egér-ellenanyagot), melyben csak a immunglobulin-molekula variábilis (antigénhez kötődő) része származott az egérből, a többi emberi eredetű volt.[17][18] Mivel kisebb mellékhatások így is előfordultak, újabban a terápiás monoklonális ellenanyagok teljesen humán eredetűek, vagyis olyan transzgénikus egerekben fejlesztik őket, amelyek immunglobulin-génjeit emberire cserélték.[19]

Felhasználása
[szerkesztés]Diagnosztikus tesztek, analitikai eljárások
[szerkesztés]Egy adott molekula ellen készített monoklonális ellenanyagok a későbbiekben felhasználhatóak a molekula detektálására. Jellemzően fehérjéket detektálnak így, Western blot vagy immuno dot blot módszerrel. Az immunhisztokémiai vizsgálatok során monoklonális ellenanyagokkal mutatják ki a fixált szövettani metszetekben az egyes antigéneket, amelyeket a fagyasztott mintákban vagy élő sejtekben immunfluoreszcenciával lehet detektálni.
A keverékekből immunprecipitációs eljárással lehet kiválasztani a kívánt vegyületet.
Terápiás felhasználás
[szerkesztés]A monoklonális ellenanyagok különböző módokon segíthetnek a betegségek gyógyításában, például blokkolhatnak bizonyos biokémiai folyamatokat, apoptózist indukálhatnak a célmolekulát hordozó sejtekben, megváltoztathatják a szervezet biokémiai szignáljait.[20][21]
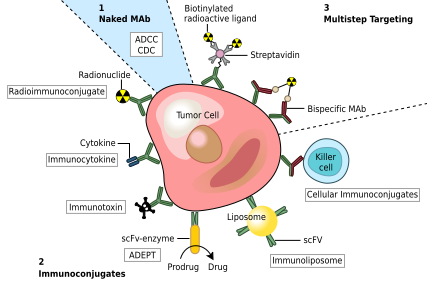
A tumorok kezelésének egyik módja, hogy monoklonális ellenanyagokat kapcsolnak a tumorspecifikus sejtfelszíni molekulákhoz, így a sejtek ellen immunválasz indukálható. Más esetekben az ellenanyaghoz toxin, radioaktív izotóp, citokin, esetleg egy másik ellenanyag köthető; utóbbival a szervezet egy másik fehérjéje vagy sejtje kapcsolható a célsejthez.
A TNF-α szignálproteinhez kötő infliximab és adalimumab fantázianevű monoklonális ellenanyagokat olyan autoimmun betegségek kezeléséhez használják, mint a rheumatoid arthritis, Crohn-betegség, fekélyes vastagbélgyulladás vagy Bechterew-kór.[23] A basiliximab és a daclizumab az interleukin 2-t blokkolja, így megelőzi az átültett szervek (pl. vese) kilökődését.[23] Az immunglobulin E-hez kötő omalizumab a súlyos allergiás asztmarohamok enyhítésére alkalmas.
2021-ben úgy tapasztalták, hogy koronavírusos betegek esetében a bamlanivimab/etesevimab és casirivimab/imdevimab monoklonális antitest alapú gyógyszerek adagolásával csökkenteni lehet a kórházi ápolás idejét és a halálozás esélyét,[24][25] így az Egyesült Államokban engedélyezték használatukat Covid19 esetén.[24][25] Később az in vitro neutralizálási tesztek során kiderült, hogy a monoklonális ellenanyag alapú gyógyszerek (a sotrovimab és tixagevimab/cilgavimab kivételével) nem hatékonyak az omikron variánssal szemben.[26]
Az alábbi táblázatban néhány terápiás monoklonális ellenanyag jellemzői láthatók:
| Típus | Név | Kórkép | Mechanizmus | Eredet |
|---|---|---|---|---|
| Gyulladáscsökkentő | infliximab[23] | gátolja a TNF-α-t | kiméra | |
| adalimumab | gátolja a TNF-α-t | humán | ||
| ustekinumab | gátolja az interleukin IL-12-t és IL-23-at | humán | ||
| basiliximab[23] |
|
gátolja az IL-2-t az aktivált T-sejteken | kiméra | |
| daclizumab[23] |
|
gátolja az IL-2-t az aktivált T-sejteken | humanizált | |
| omalizumab |
|
gátolja az immunglobulin E-t (IgE) | humanizált | |
| Rákellenes | gemtuzumab[23] | a CD33 molekulához kötődik a leukémiás sejtek felszínén | humanizált | |
| alemtuzumab[23] |
|
a CD52 molekulához kötődik a T- és B-sejtek felszínén | humanizált | |
| rituximab[23] |
|
a CD20 mokelulához kötődik a B-limfociták felszínén | kiméra | |
| trastuzumab |
|
a HER2/neu onkogén receptorához kötődik | humanizált | |
| nimotuzumab | EGFR inhibitor | humanizált | ||
| cetuximab |
|
EGFR inhibitor | kiméra | |
| bevacizumab, ranibizumab |
|
VEGF inhibitor | humanizált | |
| Rák- és vírusellenes | bavituximab[27] |
|
immunterápia, célpontja a foszfatidil-szerin[27] | kiméra |
| Anti-viral |
|
immunterápia, a SARS-CoV-2 felszíni fehérjéjéhez köt | kiméra | |
| bamlanivimab/etesevimab[24] |
|
immunterápia, a SARS-CoV-2 felszíni fehérjéjéhez köt | kiméra | |
| Sotrovimab[28] |
|
immunterápia, a SARS-CoV-2 felszíni fehérjéjéhez köt | kiméra | |
| Egyéb | palivizumab[23] |
|
gátolja a vírus fúziós proteinjét | humanizált |
| abciximab[23] |
|
gátolja a vérlemezkék GpIIb/IIIa receptorát | kiméra |
Mellékhatások
[szerkesztés]Egyes monklonális antitestek (pl. a bevacizumab és a cetuximab) különböző - súlyos és kevésbé súlyos - mellékhatásokat váltanak ki,[29][30] gyakran előfordul például szédülés, fejfájás, allergiás reakció, hasmenés vagy székrekedés, köhögés, láz, levertség, álmatlanság;[31] ritkán pedig súlyos kórképek is fellphetnek, mint anafliaxiás sokk, vérrögképződés, vérzés, a pajzsmirigy vagy a máj működésének zavarai, esetleg különböző gyulladások.[31]
Jegyzetek
[szerkesztés]- ↑ Cytochrome P450 Mediated Drug and Carcinogen Metabolism using Monoclonal Antibodies. home.ccr.cancer.gov . (Hozzáférés: 2018. április 2.)
- ↑ Gelboin HV, Krausz KW, Gonzalez FJ, Yang TJ (1999. november 1.). „Inhibitory monoclonal antibodies to human cytochrome P450 enzymes: a new avenue for drug discovery”. Trends in Pharmacological Sciences 20 (11), 432–438. o. DOI:10.1016/S0165-6147(99)01382-6. PMID 10542439.
- ↑ Waldmann, Thomas A. (1991. június 21.). „Monoclonal Antibodies in Diagnosis and Therapy” (angol nyelven). Science 252 (5013), 1657–1662. o. DOI:10.1126/science.2047874. PMID 2047874.
- ↑ (2021. december 23.) „Time to knock monoclonal antibodies off the platform for patients hospitalised with COVID-19” (english nyelven). The Lancet Infectious Diseases. DOI:10.1016/S1473-3099(21)00762-3. ISSN 1473-3099. PMID 34953521. PMC 8700277.
- ↑ (1994. július 1.) „Monoclonal antibodies: a witness seminar in contemporary medical history”. Medical History 38 (3), 322–27. o. DOI:10.1017/s0025727300036632. PMID 7934322. PMC 1036884.
- ↑ (1973. augusztus 1.) „Human x mouse somatic cell hybrid clone secreting immunoglobulins of both parental types”. Nature 244 (5416), 444–47. o. DOI:10.1038/244444a0. PMID 4200460.
- ↑ a b c The Story of César Milstein and Monoclonal Antibodies. WhatisBiotechnology.org . (Hozzáférés: 2020. szeptember 23.)
- ↑ Riechmann L, Clark M, Waldmann H, Winter G (1988. március 1.). „Reshaping human antibodies for therapy”. Nature 332 (6162), 323–27. o. DOI:10.1038/332323a0. PMID 3127726.
- ↑ (2018. november 1.) „A Nobel Prize-worthy pursuit: cancer immunology and harnessing immunity to tumour neoantigens”. Immunology 155 (3), 283–84. o. DOI:10.1111/imm.13008. PMID 30320408. PMC 6187215.
- ↑ Yang J1, Shen MH. "Polyethylene glycol-mediated cell fusion". Methods Mol Biol. 2006; 325:59–66.
- ↑ National Research Council (US) Committee on Methods of Producing Monoclonal Antibodies. Recommendation 1: Executive Summary: Monoclonal Antibody Production. Washington (DC): National Academies Press (US); 1999. ISBN 978-0-309-07511-4
- ↑ (2018. június 1.) „Inaugural Editorial: Searching for Magic Bullets”. Antibody Therapeutics 1 (1), 1–5. o. DOI:10.1093/abt/tby001. PMID 30101214. PMC 6086361.
- ↑ (2019. augusztus 1.) „Functional diversification of hybridoma-produced antibodies by CRISPR/HDR genomic engineering”. Science Advances 5 (8), eaaw1822. o. DOI:10.1126/sciadv.aaw1822. PMID 31489367. PMC 6713500.
- ↑ (2002. január 1.) „Recombinant monoclonal antibody technology”. Transfusion Clinique et Biologique 9 (1), 15–22. o. DOI:10.1016/S1246-7820(01)00210-5. PMID 11889896.
- ↑ Dr. George Pieczenik. LMB Alumni. MRC Laboratory of Molecular Biology (LMB), 2009. szeptember 17. [2012. december 23-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. november 17.)
- ↑ (2000) „Phage display: a molecular tool for the generation of antibodies – a review”. Placenta 21 Suppl A (Suppl A), S106–12. o. DOI:10.1053/plac.1999.0511. PMID 10831134.
- ↑ (1984. február 12.) „Production of functional chimaeric mouse/human antibody”. Nature 312 (5995), 643–46. o. DOI:10.1038/312643a0. PMID 6095115.
- ↑ (2001. április 1.) „Therapeutic antibody expression technology”. Current Opinion in Biotechnology 12 (2), 188–94. o. DOI:10.1016/S0958-1669(00)00198-1. PMID 11287236.
- ↑ (1995) „Human antibodies from transgenic mice”. International Reviews of Immunology 13 (1), 65–93. o. DOI:10.3109/08830189509061738. PMID 7494109.
- ↑ (2000. február 1.) „Therapeutic monoclonal antibodies”. Lancet 355 (9205), 735–40. o. DOI:10.1016/S0140-6736(00)01034-5. PMID 10703815.
- ↑ Australian Prescriber (2006). „Monoclonal antibody therapy for non-malignant disease”. Australian Prescriber 29 (5), 130–33. o. DOI:10.18773/austprescr.2006.079.
- ↑ (2001. november 1.) „Improving the efficacy of antibody-based cancer therapies”. Nature Reviews. Cancer 1 (2), 118–29. o. DOI:10.1038/35101072. PMID 11905803.
- ↑ a b c d e f g h i j Pharmacology. Edinburgh: Churchill Livingstone, 241, for the examples infliximab, basiliximab, abciximab, daclizumab, palivusamab, gemtuzumab, alemtuzumab and rituximab, and mechanism and mode. o. (2003). ISBN 978-0-443-07145-4
- ↑ a b c (9 February 2021). "FDA Authorizes Monoclonal Antibodies for Treatment of COVID-19". Sajtóközlemény.
 Ez a cikk ebből a forrásból származó szöveget tartalmaz, amely közkincs.
Ez a cikk ebből a forrásból származó szöveget tartalmaz, amely közkincs.
- ↑ a b c (21 November 2020). "Coronavirus (COVID-19) Update: FDA Authorizes Monoclonal Antibodies for Treatment of COVID-19". Sajtóközlemény.
 Ez a cikk ebből a forrásból származó szöveget tartalmaz, amely közkincs.
Ez a cikk ebből a forrásból származó szöveget tartalmaz, amely közkincs.
- ↑ (2021. december 1.) „Omicron overpowers key COVID antibody treatments in early tests”. Nature. DOI:10.1038/d41586-021-03829-0. PMID 34937889.
- ↑ a b Staff, Adis Insight. Bavituximab profile Last updated 27 January 2016
- ↑ Emergency Use Authorization letter (PDF). U.S. Food and Drug Administration (FDA) , 2021. december 16. (Hozzáférés: 2022. január 6.)
 Ez a cikk ebből a forrásból származó szöveget tartalmaz, amely közkincs.
Ez a cikk ebből a forrásból származó szöveget tartalmaz, amely közkincs.
- ↑ Monoclonal antibodies to treat cancer | American Cancer Society. www.cancer.org . (Hozzáférés: 2018. április 19.)
- ↑ „Monoclonal antibody drugs for cancer: How they work”, Mayo Clinic (Hozzáférés: 2018. április 19.)
- ↑ a b „Monoclonal Antibodies: List, Types, Side Effects & FDA Uses (Cancer)”, MedicineNet (Hozzáférés: 2018. április 19.)
Fordítás
[szerkesztés]- Ez a szócikk részben vagy egészben a Monoclonal antibody című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
