Metántiol
| Metántiol | |||
| |||
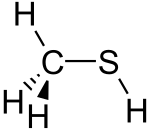
 2 dimenziós szerkezet |
 3 dimenziós szerkezet | ||
| IUPAC-név | Metántiol | ||
| Más nevek | metil-merkaptán | ||
| Kémiai azonosítók | |||
| CAS-szám | 74-93-1 | ||
| ChemSpider | 855 | ||
| KEGG | C00409 | ||
| ChEBI | 16007 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | CH4S | ||
| Moláris tömeg | 48,11 g/mol | ||
| Szag | fokhagymaszagú | ||
| Olvadáspont | −123 °C | ||
| Forráspont | 5,95 °C | ||
| Oldhatóság (vízben) | 2% | ||
| Oldhatóság | alkohol, éter | ||
| Savasság (pKa) | ~10,4 | ||
| Veszélyek | |||
| EU osztályozás | |||
| NFPA 704 | |||
| R mondatok | R12, R23, R50/53 | ||
| S mondatok | S16, S25, S33S60, S61 | ||
| Rokon vegyületek | |||
| Rokon vegyületek | etántiol | ||
| Az infoboxban SI-mértékegységek szerepelnek. Ahol lehetséges, az adatok standardállapotra (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. Az ezektől való eltérést egyértelműen jelezzük. | |||
A metántiol vagy metil-merkaptán szerves vegyület, képlete CH3SH. A legegyszerűbb tiol, benne a tiolcsoporthoz egy metilcsoport kapcsolódik. Standard körülmények között színtelen, bűzös (fokhagymára emlékeztető szagú), erősen gyúlékony gáz. Többek között ez felelős a rossz szájszagért. Mivel szagát az ember már igen kis koncentrációban is érzi, gyakran adják földgázhoz a robbanásveszély megelőzése érdekében.
Kémiai tulajdonságok
[szerkesztés]Szerkezete hasonló a metanoléhoz, ugyanúgy tetraéderes a szénatomnál, de a kénnél a kötésszög csak 100° körüli (a metanolban 109°)[1][2] Gyenge (a metanolnál több nagyságrenddel erősebb) sav, pKs értéke körülbelül 10,4. Savas tulajdonságának köszönhetően töményebb lúgoldatokkal sóképzés közben reagál. Enyhe oxidációja hidrogénelvonással jár, és dimetil-diszulfid képződéséhez vezet.
- 2CH3SH + [O] → CH3SSCH3 + H2O
További oxidáció során metánszulfonsavvá oxidálható.
Előállítás
[szerkesztés]Előállítása iparilag metanol és hidrogén-szulfid gáz reakciójával történik alumínium-oxid katalizátor jelenlétében.[3]
- CH3OH + H2S → CH3SH + H2O
Források
[szerkesztés]- ↑ http://cccbdb.nist.gov/exp2.asp?casno=74931
- ↑ http://cccbdb.nist.gov/exp2.asp?casno=67561
- ↑ Thiols, Kirk-Othmer Concise Encylclopedia of Chemical Technology, 3rd, New York: John Wiley & Sons, Inc., 946–963. o. (1988). ISBN 978-0471801047

