Kolecisztokinin
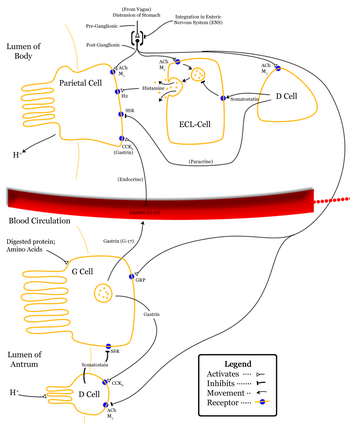
A kolecisztokinin (rövidítve CCK; jelentése epehólyagmozgató) egy emésztőrendszeri peptidhormon, amelynek elsődleges funkciója, hogy elősegítse a zsírok és fehérjék emésztését. A korábban pankreoziminnek is nevezett peptid a nyombél enteroendokrin sejtjeiben képződik.[1] és hatására a hasnyálmirigyből emésztőenzimek, az epehólyagból pedig epe szabadul fel. Csökkenti az étvágyat is.
Szerkezete
[szerkesztés]A kolecisztokinin génje, a CCK a 3. kromoszómán található. A prekurzor fehérje utólagos módosításokon megy át, ennek hatására több, különböző hosszúságú, aktív kolecisztokinin-molekula jön létre: a CCK58, CCK33, CCK22 és CCK8, ahol a szám a peptidet alkotó aminosavak számát jelenti. Szerkezetében nagyon hasonlít a szintén az emésztést befolyásoló gasztrinra, a C-terminus felőli öt aminosavban megegyeznek. A C-terminus felőli 7. tirozin aminosavhoz szulfátcsoport kapcsolódik: ez létfontosságú ahhoz, hogy a hormon kapcsolódni tudjon a receptorához. Előfordulnak szulfátmentes kolecisztokininek is, de azok nem képesek aktiválni a receptort.[2]
Funkciója
[szerkesztés]A kolecisztokinin az emésztés folyamatát és az étvágyat befolyásolja. A vékonybél (ezen belül a nyombél és az éhbél) enteroendokrin sejtjei, az ún. I-sejtek, az enterális idegrendszer neuronjai és az agy termeli. Szekrécióját legnagyobb mértékben a vékonybélbe lépő gyomortartalom zsírsav és aminosav összetevői indukálják, kisebb részben pedig a bélnyálkahártya sejtjei által termelt kolecisztokinin-felszabadító peptid, a hasnyálmirigy acináris sejtjei termelt monitor peptid és a bolygóideg paraszimpatikus idegvégződésein felszabaduló acetilkolin is aktiválja.
A kolecisztokinin csökkenti a gyomorkiürülés sebességét és visszafogja a gyomorsav termelődését. Hatására a hasnyálmirigy acináris sejtjei emésztőenzimekben gazdag szekrétumot választanak ki. Ezek az enzimek meggyorsítják a bélben a zsírok, fehérjék és szénhidrátok lebontását. Amint ezen tápanyagok elfogynak a bélűrben, a hormontermelés is mérséklődik. A kolecisztokinin kibocsátását gátolja még a szomatosztatin és a hasnyálmirigy-peptid. Az acináris sejtek által elválasztott fehérjebontó tripszin enzim lebontja a kolecisztokinin-felszabadító proteint és a monitor proteint, negatív visszacsatolással csökkentve a kolecisztokinin és azon keresztül a saját szintjét is.
A hormon elősegíti az epe termelődését és az epehólyag kiürülését. Utóbbiban mind a hólyag összehúzódásait, mind az Oddi-záróizom elernyedését indukálja; ezáltal az epe az epehólyagból a vékonybélbe áramlik.
Idegrendszeri hatása
[szerkesztés]Az agyban is megtalálható receptorain keresztül a kolecisztokinin pozitív hatással van a jóllakottságérzetre. Egyes források szerint mestersége beadása hányingert és szorongást is okoz, bár a különböző hosszúságú CCK-knak változó a hatása.[3] Az éhségérzet csökkentését feltehetően a gyomor kiürülésének lassításával éri el.[4]
A kolecisztokinin stimuláló hatással van a bolygóidegre; ezt a hatást a kapszaicin gátolja.[5] A stimulációs effektus kioltja az "éhséghormon", a ghrelin gátlóhatását az idegen.[6] A mesterséges, négy aminosavból (Trp-Met-Asp-Phe-NH2) álló CKK-4 szorongást idéz elő, amit a pánikrohamok elleni gyógyszerek kutatásában is felhasználnak.[7] Egy vizsgálat szerint a kolecisztokininnek szerepe lehet a Parkinson-kórban tapasztalt hallucinációk előidézésében.[8]
A hormonnak két receptora van: a kolecisztokinin A receptor a hasnyálmirigy acináris sejtjeiben, a B pedig az agyban és a gyomorban található. A B receptor a gasztrint is képes megkötni, amely a gyomorsav termelését segíti elő.[9][10][11]
Kimutatták, hogy a kolecisztokinin kapcsolatba léphet az orexintermelő (az orexin az étvágyat és az alvást szabályozó neuropeptid) idegsejtekkel,[12] így közvetetten hatással lehet az alvás-ébrenlét ciklusra.[13]
Egy vizsgálat szerint a kolecisztokinin fontos szerepet játszhat az idegrendszer opiátokhoz (morfium, heroin) való hozzászokásában és legalább részben felelős a megvonás során jelentkező fájdalomérzet-túlérzékenység kiváltásáért.[14][15]
A nagy molekulasúlyú kolecisztokinin nem képes áthatolni a vér-agy gáton, de az agytörzs és a hipotalamusz egyes része kívül esnek a gáton.
Jegyzetek
[szerkesztés]- ↑ Cholecystokinin. Colorado State University, 2001. január 28. [2016. március 17-i dátummal az eredetiből archiválva]. (Hozzáférés: 2015. november 6.)
- ↑ (2014) „Measurement of nonsulfated cholecystokinins”. Scand. J. Clin. Lab. Invest. 74 (5), 424–31. o. DOI:10.3109/00365513.2014.900695. PMID 24734780.
- ↑ (1998) „Untangling the effects of hunger, anxiety, and nausea on energy intake during intravenous cholecystokinin octapeptide (CCK-8) infusion”. Physiol. Behav. 65 (2), 303–10. o. DOI:10.1016/S0031-9384(98)00169-3. PMID 9855480.
- ↑ (1987) „Proglumide, a cholecystokinin antagonist, increases gastric emptying in rats”. Am. J. Physiol. 252 (2 Pt 2), R353-60. o. [2008. július 24-i dátummal az eredetiből archiválva]. PMID 3812772. (Hozzáférés: 2016. augusztus 1.)
- ↑ (1998. július 1.) „Neural injury, repair, and adaptation in the GI tract. II. The elusive action of capsaicin on the vagus nerve”. Am. J. Physiol. 275 (1 Pt 1), G8-13. o. [2016. június 29-i dátummal az eredetiből archiválva]. PMID 9655678. (Hozzáférés: 2016. augusztus 1.)
- ↑ (2005. március 1.) „CCK inhibits the orexigenic effect of peripheral ghrelin”. Am. J. Physiol. Regul. Integr. Comp. Physiol. 288 (3), R751-8. o. DOI:10.1152/ajpregu.00094.2004. PMID 15550621.
- ↑ (1993. július 1.) „Neurobiological investigations into the role of cholecystokinin in panic disorder”. J Psychiatry Neurosci 18 (4), 178–88. o. PMID 8104032. PMC 1188527.
- ↑ (2003. június 1.) „Cholecystokinin, cholecystokinin-A receptor and cholecystokinin-B receptor gene polymorphisms in Parkinson's disease.”. Pharmacogenetics 13 (6), 365–9. o. DOI:10.1097/00008571-200306000-00008. PMID 12777967.
- ↑ (2005. január 1.) „Distinct molecular mechanisms for agonist peptide binding to types A and B cholecystokinin receptors demonstrated using fluorescence spectroscopy”. J. Biol. Chem. 280 (2), 1044–50. o. DOI:10.1074/jbc.M409480200. PMID 15520004.
- ↑ (2004. március 1.) „In vitro and in vivo evaluation of 111In-DTPAGlu-G-CCK8 for cholecystokinin-B receptor imaging”. J. Nucl. Med. 45 (3), 485–94. o. PMID 15001692.
- ↑ (2003. május 1.) „Identification of tyrosine 189 and asparagine 358 of the cholecystokinin 2 receptor in direct interaction with the crucial C-terminal amide of cholecystokinin by molecular modeling, site-directed mutagenesis, and structure/affinity studies”. Mol. Pharmacol. 63 (5), 973–82. o. DOI:10.1124/mol.63.5.973. PMID 12695525.
- ↑ (2005. augusztus 1.) „Cholecystokinin activates orexin/hypocretin neurons through the cholecystokinin A receptor”. J. Neurosci. 25 (32), 7459–69. o. DOI:10.1523/JNEUROSCI.1193-05.2005. PMID 16093397.
- ↑ Kapas, Levente (2010), Metabolic signals in sleep regulation: the role of cholecystokinin, University of Szeged, <http://www.phd.szote.u-szeged.hu/Elmeleti_DI/Disszertaciok/2010/de_Levente_Kapas.pdf>
- ↑ (2000) „Acute tolerance to continuously infused alfentanil: the role of cholecystokinin and N-methyl-D-aspartate-nitric oxide systems”. Anesth. Analg. 91 (1), 110–6. o. DOI:10.1097/00000539-200007000-00021. PMID 10866896.
- ↑ (2007) „Activation of spinal cholecystokinin and neurokinin-1 receptors is associated with the attenuation of intrathecal morphine analgesia following electroacupuncture stimulation in rats”. J. Pharmacol. Sci. 104 (2), 159–66. o. DOI:10.1254/jphs.FP0070475. PMID 17558184.
Fordítás
[szerkesztés]- Ez a szócikk részben vagy egészben a Cholecystokinin című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
