Galaktóz
| Galaktóz | |
 |

|
| |
| Szabályos név | (2R,3S,4S,5R)-2,3,4,5,6-pentahidroxihexanal |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | 26566-61-0 |
| PubChem | 6036 |
| MeSH | Galactose |
| ATC kód | V04CE01 |
| Gyógyszer szabadnév | galactose |
| Gyógyszerkönyvi név | Galactosum |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | C6H12O6 |
| Moláris tömeg | 180,155 g/mol[1] |
| Olvadáspont | 170 °C[1] |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
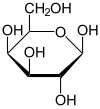
A galaktóz (Gal) egy monoszacharid, amely kevésbé édes, mint a glükóz, és kevésbé vízoldékony. A növény- és az állatvilágban is megtalálható kötött állapotban, elterjedt. A galaktóz polimereit galaktánoknak nevezik; a hemicellulózban találhatóak, és hidrolízissel galaktózzá alakíthatók. Galaktóztartalmú poliszacharidok találhatók egyes fák mézgájában és algákban. A galaktóz és a glükóz a diszacharid laktóz két monoszacharid alkotórésze. Más olighoszacharidokban is előfordul (például melibióz, raffinóz). Megtalálható egyes agyban és idegsejtekben előforduló lipidekben is (cerebrozidok, gangliozidok).
A laktóz hidrolízisét a laktáz enzim katalizálja, amely β-galaktozidáz. Az emberi testben a glükóz galaktózzá alakul az emlőben a tejelválasztás során, amikor az emlőmirigyek laktózt szekretálnak. Innen a neve: galaktosz (γάλακτος) görögül tejet jelent.[2]
Kémiai tulajdonságai
[szerkesztés]Hideg vizes oldatból a galaktóz piranózgyűrűs alakjának α-, hideg alkoholos oldatból a β-anomerje kristályosítható ki. Léteznek öttagú furanózgyűrűt tartalmazó származékai is.
A galaktóz redukciójakor egy hatértékű alkohol, dulcit keletkezik. A dulcit hat szénatomos cukoralkohol, hexit. A növényvilágban fordul elő. Szimmetrikus szerkezetű, ezért optikailag inaktív. Optikai inaktivitása miatt mezo-dulcitnak is szokás nevezni.
Az egyensúlyi vizes oldatában előforduló 5 tautomer a következő:[3]
- d-galaktóz (nyílt láncú): 0,02%
- α-d-galaktopiranóz: 30%
- β-d-galaktopiranóz: 64%
- α-d-galaktofuranóz: 2,5%
- β-d-galaktofuranóz: 3,5%
Jegyzetek
[szerkesztés]- ↑ a b William M. Haynes. CRC Handbook of Chemistry and Physics, 97th edition, Boca Raton: CRC Press, 3-280. o. (2016). ISBN 978-1-4987-5429-3
- ↑ Fülöp József: Rövid kémiai értelmező és etimológiai szótár. Celldömölk: Pauz–Westermann Könyvkiadó Kft. 1998. 54. o. ISBN 963 8334 96 7
- ↑ Peter M. Collins. Dictionary of Carbohydrates, 2nd edition, Boca Raton: Chapman & Hall/CRC, 513. o. (2006). ISBN 978-0-8493-3829-8
