Ftálimid-kálium
Megjelenés
| Ftálimid-kálium | |

| |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | 1074-82-4 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | C8H4KNO2 |
| Moláris tömeg | 185,2 g/mol |
| Megjelenés | világossárga szilárd anyag |
| Sűrűség | 1,63 g/cm³[1] |
| Olvadáspont | > 300 °C (bomlik) |
| Forráspont | 366 °C[1] |
| Oldhatóság (vízben) | oldódik |
| Veszélyek | |
| EU osztályozás | nincsenek veszélyességi szimbólumok[1] |
| NFPA 704 | |
| R mondatok | (nincs)[1] |
| S mondatok | (nincs)[1] |
| Rokon vegyületek | |
| Rokon vegyületek | Ftálimid |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
A ftálimid-kálium szerves vegyület, a ftálimid káliumsója, képlete C8H4KNO2.
Tulajdonságai
[szerkesztés]Többnyire pelyhes, fehér kristályokat alkot. Vízben oldható, de nedvességre érzékeny, bomlik. Bázikus tulajdonságú anyag. Olvadáspontja 300 °C feletti, ahol bomlásnak indul.
Előállítása
[szerkesztés]Kálium-hidroxid oldatához forró ftálimid-oldatot adnak, a kívánt termék az oldatból kiválik.[2]
Felhasználása
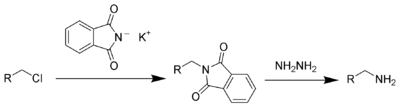
[szerkesztés]A ftálimid-kálium -NH2-szinton, ami lehetővé teszi alkil-halidokkal (Gabriel-szintézis) vagy alkoholokkal (Mitsunobu-reakció) reagáltatva primer aminok előállítását. Az alkilezéssel a nukleofilitását elveszti, nem reagál tovább. A termék bázissal (pl. NaOH) vagy hidrazinnal hasítható, az utóbbival stabil, könnyen kezelhető ciklikus melléktermék jön létre:
Tipikus reakciókörülmények
[szerkesztés]- Gabriel-szintézis: 2 ekvivalens XR és KOH; [bmim]BF4; 40 vagy 80 °C; 2-5 óra.[3]
- Mitsunobu-reakció: ROH és 1.3 ekvivalens ftálimid-kálium, DIAD, PPh3; THF, szobahőmérséklet; 4 óra.[4]
Jegyzetek
[szerkesztés]- ↑ a b c d e A ftálimid-kálium vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2011. 02. 03. (JavaScript szükséges) (angolul)
- ↑ P. L. Salzberg and J. V. Supniewski (1941). „β-Bromoethylphthalimide”. Org. Synth..; Coll. Vol. 1: 119
- ↑ Organic Reactions in Ionic liquids: N-Alkylation of Phthalimide and Several Nitrogen Heterocycles Z.-G. Le, Z.-C. Chen, Y. Hu, Q.-G. Zheng, Synthesis, 2004, 208-212.
- ↑ A convenient Two-Step Procedure for the Synthesis of Substituted Allylic Amines from Allylic Alcohols S. E. Sen, S. L. Roach, Synthesis, 1995, 756-758.