Szerkesztő:Alfa-ketosav/Fenil-szalicilát
| Fenil-szalicilát[1] | |||
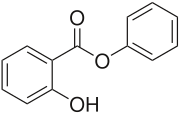 Skeletal formula | |||
 Pálcikamodell | |||
| Más nevek | Szalol | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 118-55-8 | ||
| PubChem | 8361 | ||
| ChemSpider | 8058 | ||
| EINECS-szám | 204-259-2 | ||
| KEGG | C14163 | ||
| MeSH | C026041 | ||
| ChEBI | 34918 | ||
| ATC kód | G04BX12 | ||
| |||
| |||
| InChIKey | ZQBAKBUEJOMQEX-UHFFFAOYSA-N | ||
| UNII | 28A37T47QO | ||
| ChEMBL | 1339216 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C13H10O3 | ||
| Moláris tömeg | 214.22 g/mol | ||
| Megjelenés | White solid | ||
| Sűrűség | 1,25 g/cm3 | ||
| Olvadáspont | 41,5 °C | ||
| Forráspont | 173 °C | ||
| Oldhatóság (vízben) | 0,15 g/l | ||
| Mágneses szuszceptibilitás | -123,2·10−6 cm3/mol | ||
| Törésmutató (nD) | 1,615[2] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A fenil-szalicilát, más néven szalol (C6H5COOC6H4OH) fehér szilárd anyag. Néha használatos napvédő krémekben és antiszeptikumként.
Szintézise és reakciói
[szerkesztés]A fenil-szalicilátot először 1883-ban állította elő Marceli Nencki, aki kutatásait nem közölte, és tőle függetlenül 1885-ben Richard Seifert, aki kutatásait közölte. Előállítható szalicilsav és fenol keverékének hevítésével foszforil-klorid jelenlétében.[3] Szalicilsav hevítésekor is keletkezik:[4]
E reakció során a szalicilsav dehidratálódik és dekarboxileződik. A fenil-szalicilátból hevítéskor xanton keletkezik:[5][6]
Ebben a reakcióban fenol és szén-dioxid is keletkezik.
Szalolreakció
[szerkesztés]A szalolreakcióban a fenil-szalicilát o-toluidinnel reagál 1,2,4-triklórbenzolban magas hőmérsékleten, o-szaliciltoluid keletkezése közben.[7]
Használata
[szerkesztés]Antiszeptikumként használták.[8]
Enyhe analgetikumként hat.[9]
Története
[szerkesztés]Hermann Sahli svájci háziorvos a reumatoid arthritisre használt nátrium-szalicilátot helyettesítő vegyületet kívánt, mert a nátrium-szalicilát egyes betegeknél mellékhatásokat váltott ki.
Jegyzetek
[szerkesztés]- ↑ Merck Index, 11th Edition, 7282.
- ↑ a b ChemBK Chemical Database
- ↑ (1952) „p-Chlorophenyl Salicylate”. Organic Syntheses 32, 25. o. DOI:10.15227/orgsyn.032.0025.
- ↑ (2004) „Selective Synthesis of Phenyl Salicylate (Salol) by Esterification Reaction over Solid Acid Catalysts”. Journal of Molecular Catalysis A: Chemical 223 (1–2), 155–159. o. DOI:10.1016/j.molcata.2004.03.057.
- ↑ A. F. Holleman (1927). „Xanthone”. Org. Synth. 7, 84. o. DOI:10.15227/orgsyn.007.0084.
- ↑ Salicylic Acid, Ullmann's Encyclopedia of Industrial Chemistry. DOI: 10.1002/14356007.a23_477 (2000). ISBN 3527306730
- ↑ (1946) „SALICYL-o-TOLUIDE”. Org. Synth. 26, 92. o.; Coll. Vol. 3: 765
- ↑ Walter Sneader. Drug discovery: a history. John Wiley and Sons, 358–. o. (2005). ISBN 978-0-471-89980-8
- ↑ Judith Barberio. Nurse's Pocket Drug Guide, 2010. McGraw Hill Professional, 57–. o. (2009. szeptember 4.). ISBN 978-0-07-162743-6
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Phenyl salicylate című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.


