Rénium-heptoxid
| Rénium-heptoxid | |||
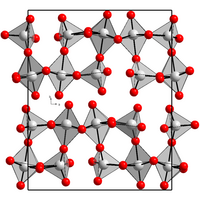 Rénium-heptoxid | |||

| |||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 1314-68-7 | ||
| PubChem | 123106 | ||
| EINECS-szám | 215-241-9 | ||
| |||
| |||
| InChIKey | NBGOSNNAAHDRLK-UHFFFAOYSA-N | ||
| UNII | 0DJ421156F | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | Re2O7 | ||
| Moláris tömeg | 484,40298 g/mol | ||
| Megjelenés | sárga kristályos por | ||
| Sűrűség | 6,103 g/cm3, szilárd | ||
| Olvadáspont | 360 °C | ||
| Forráspont | szublimál | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A rénium-heptoxid szervetlen vegyület, képlete Re2O7. Sárga szilárd anyag, a HOReO3 anhidridje. A perréniumsav (Re2O7·2H2O) szorosan kapcsolódik hozzá. Számos réniumvegyület előállítható belőle, és ez az érc pörkölésekor keletkező illékony frakció.[2]
Szerkezet
[szerkesztés]A szilárd Re2O7 váltakozó oktaéderes és tetraéderes Re központokból áll. Hevítéskor a polimer molekuláris Re2O7-dá bomlik. Ez az anyag hasonlít a mangán-heptoxidra, és két közös csúcsú ReO4 tetraéderből áll, vagyis szerkezete O3Re–O–ReO3.[3]
Szintézise, reakciói
[szerkesztés]A rénium-heptoxid rénium, rénium-oxidok vagy -szulfidok levegőn 500-700 °C-on történő oxidációjakor keletkezik.[4]
A Re2O7 vízben reagál, perréniumsavat adva.
A Re2O7 hevítése rénium-dioxidot eredményez, melyet a sötétkék szín is jelez:[5]
Ón-tetrametillel oxidációs reakciók katalizátorává, metilrénium-trioxiddá alakul:[6]
Egy hasonló reakcióban hexametil-disziloxánnal reagál sziloxidot eredményezve:[4]
Használata
[szerkesztés]Hidrogénezéshez
[szerkesztés]A rénium-heptoxidot etenolízis,[7] karbonil- és amidredukció katalízisére használják.[8]
Jegyzetek
[szerkesztés]- ↑ Rhenium(VII) oxide (angol nyelven). pubchem.ncbi.nlm.nih.gov . (Hozzáférés: 2021. december 14.)
- ↑ Ullmann Vegyipari Enciklopédia
- ↑ Wells, A.F.. Structural Inorganic Chemistry. Clarendon Press (1984). ISBN 0-19-855370-6
- ↑ a b Trimethylsilyl Perrhenate, Inorganic Syntheses, 149–151. o.. DOI: 10.1002/9780470132401.ch40 (1967). ISBN 9780470132401
- ↑ O. Glemser.szerk.: G. Brauer: Rhenium, Handbook of Preparative Inorganic Chemistry, 2nd, Academic Press, 1476-1485. o. (1963)
- ↑ (1997) „Organorhenium Oxides”. Acc. Chem. Res. 30 (4), 169–180. o. DOI:10.1021/ar9601398.
- ↑ Metathesis, Kirk-Othmer Encyclopedia of Chemical Technology. Wiley
- ↑ Handbook of Heterogeneous Catalytic Hydrogenation for Organic Synthesis, 1st, New York: Wiley-Interscience, 42-43, 182, 389-390, & 408. o. (2001). ISBN 9780471396987
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Rhenium(VII) oxide című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.



