Neutrofil granulocita
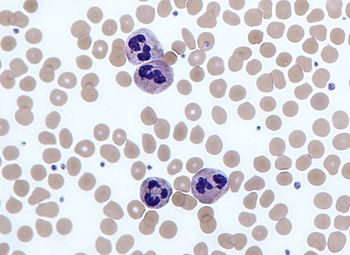

A neutrofil granulociták (vagy neutrofilek) a leggyakrabban előforduló fehérvérsejtek, a legtöbb emlősben ők teszik ki a leukociták 40-75%-át. Elsődleges funkciójuk a szervezet veleszületett immunrendszerének működtetése. Az eozinofil és bazofil sejtekkel együtt a granulociták csoportjához tartoznak.
A neutrofilek őssejtekből keletkeznek a csontvelőben. Rövid élettartamú, mozgékony sejtek, amelyek a szövetek olyan régióiba is beférkőznek, ahová az immunrendszer más sejtjei nem képesek. Két csoportjuk van, a karéjos magvú (vagy polimorfonukleáris) és a pálcikamagvú granulociták.[1][2][3] Sejtmagvuk általában 2-5 lebenyből (karéjból) áll.
Nevüket onnan kapták, hogy a vér hisztológiai festésekor citoplazmájuk sem eozint (mint a vörösre színeződő eozinofilek), sem hematoxilint (sötétkékre festődő bazofilek) nem vesz fel és mikroszkóp alatt semleges rózsaszínnek mutatkozik.
A neutrofil granulociták a falósejtek (fagociták) közé tartoznak és általában a véráramban tartózkodnak. Gyulladásos folyamat kezdetekor (legyen az bakteriális fertőzés, környezeti hatás vagy bizonyos tumorok által kiváltva),[4][5][6] az elsők között reagálnak és azonnal a gyulladás helyszínére sietnek. Olyan szignálmolekulákat követve, mint az interleukin-8 (IL-8), C5a, fMLP, leukotrién B4 vagy hidrogén-peroxid átszüremlenek a véredények falain és a kötőszövet sejtjei között.[7] Elsősorban ők alkotják a genny sejtes részét, nekik köszönhető annak sárgás-fehéres színe. Vannak olyan kórokozók, amelyet a neutrofilek nem képesek bekebelezni, ilyen esetben az immunrendszer más sejtjeire is szükségük van.
Jellemzőik
[szerkesztés]
A neutrofil granulociták átmérője a hisztológiai kenetekben 12-15 mikrométer (µm), míg szuszpenzióban átlagosan 8,85 µm-esek.[8]
Az eozinofil és bazofil granulocitákkal közösen ők alkotják a polimorfonukleáris sejtek csoportját (szemben a nem lebenyes magvú mononukleáris sejtekkel, ahová a limfociták és monociták tartoznak). Sejtmagjuk jellegzetes módon lebenyekből áll, amelyeket kromatin (a kromoszómák anyaga) köt össze. A sejt érésével sejtmagvacskája felszívódik.[9] A citoplazmában a Golgi-apparátus kicsi, kevés a riboszóma és a mitokondrium, a durva felszínű endoplazmatikus retikulum pedig hiányzik.[9] Ezenkívül mintegy 200 azurofil (Romanowsky-festéssel festhető) granulumot tartalmaz.[9]
Nőkben a neutrofilek sejtmagjai mellett megfigyelhető a dobverő alakú ún. Barr-test, egy inaktiválódott X-kromoszóma.[9]
Ahogyan a sejtek idősebbé válnak, sejtmagvuk egyre szegmentáltabb lesz. Egy átlagos neutrofil magja 3-5 lebenyből áll. A túl sok lebeny betegség (főleg B12-vitamin hiányának) jele lehet.
A neutrofilek a leggyakoribb fehérvérsejtek az emberi vérben; a leukociták mintegy 50-70%-át teszik ki. Naponta kb. tízmilliárd keletkezik belőlük. Az egészséges szervezetben koncentrációjuk 1900–8000/mikroliter. Megfigyelték, hogy az afrikai és közel-keleti származású személyek neutrofilszáma valamivel alacsonyabb.
Az inaktív, "járőröző" sejtek gömbszerűek. Miután aktiválódtak, amőbaszerűen változtatják az alakjukat és állábakat bocsátanak ki, hogy bekebelezzék a baktériumokat és sejttörmelékeket.[10]
Élettartamuk
[szerkesztés]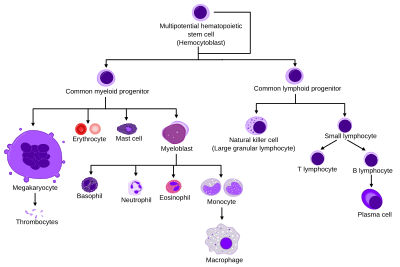
A különböző mérések 5-90 nap közé teszik a keringésben lévő neutrofilek élettartamát.[11] Aktiváció után, a szövetekben 1-2 nap után elpusztulnak.[12]
Bár rövidebb élettartamúak, jóval gyakoribbak mint a monociták/makrofágok, ezért valószínűbb, hogy egy kórokozó először velük találkozik. Egyes elméletek szerint a neutrofilek rövid élete evolúciós adaptáció, amellyel a szervezet megakadályozza, hogy a kórokozó megfertőzze őket (illetve végigvigye bennük az életciklusát). Ezenkívül, mivel gyulladás esetén a saját szöveteket is lebontják, a rövid élettartam csökkenti a gyulladás okozta károkat.[12]
Megfigyelték, hogy a miután a neutrofil megemésztett egy kórokozót, felületén olyan molekulák jelennek meg (CD-31 és foszfatidilszerin), amik miatt a makrofágok fagocitózissal felfalják őket.
Működésük
[szerkesztés]A neutrofil granulociták sejtfelszíni receptoraikkal képesek megkötni bizonyos jelzőmolekulákat (interleukin-8, gamma interferon, B4 leukotrién, a komplementrendszerből a C3a és C5a komponensek) és a koncentrációgrádienst követve megkeresni azok forrását. Ezt a folyamatot kemotaxisnak nevezzük. A szignálmolekulákat kórokozóval találkozó endoteliális sejtek, hízósejtek vagy makrofágok bocsátják ki. A helyszínre siető neutrofilek maguk is kibocsátanak olyan citokineket (pl. interleukin-1-et), amelyek más sejtekre hatva felerősítik a gyulladás folyamatát.[13] A többi sejt aktiválásán felül három fő módszerrel rendelkeznek a betolakodó baktériumok vagy más patogének leküzdésére: fagocitózis (bekebelezés), degranuláció (antimikrobiális anyagok kiválasztása) és hálószerű sejten kívüli csapdák (neutrophil extracellular trap, NET) létrehozása.[14]
Fagocitózis
[szerkesztés]A neutrofilek a falósejtek közé tartoznak, vagyis képesek részecskék bekebelezésére. A folyamat megindításához a célpont felületén fagocitózist indukáló molekuláknak, ún. opszonineknek (jellegzetes bakteriális antigénnek, odakötött antitestnek, a komplementrendszer C3b komponensének) kell jelen lennie.[10] Miután a sejt állábaival körbevette és internalizálta a mikroorganizmust, egy fagoszóma jön létre körülötte, amibe lizáló enzimek és oxidáló szabad gyököket tartalmazó molekulák kerülnek. Utóbbi miatt a fagocitózis fokozott oxigénfelvétellel jár.
Degranuláció
[szerkesztés]A neutrofil granulociták a citoplazmájukból háromféle granulum tartalmát képesek a környezetbe üríteni. Az ezekben található enzimek antimikrobiális tulajdonságúak.
| Granulum típusa | Protein |
| azurofil (vagy elsődleges) | mieloperoxidáz, baktericid/permeabilitásnövelő protein (BPI), defenzinek, a fehérjebontó neutrofil elasztáz és katepszin G |
| specifikus (vagy másodlagos) | alkalikus foszfatáz, lizozim, NADPH-oxidáz, kollagenáz, laktoferrin, hisztamináz,[15] katelicidin |
| harmadlagos | katepszin, zselatináz, kollagenáz |
Extracelluláris csapdák
[szerkesztés]2004-ben fedezték fel, hogy az aktivált neutrofilek hálószerű DNS-fehérje struktúrákat bocsátanak ki a baktériumok ellen.[16] Ezek az ún. extracelluláris csapdák (neutrophil extracellular trap, NET) a kromoszómák anyagából, a kromatinból és szerin-proteázokból épülnek fel[17] Feltételezik hogy önmagukban is képesek elpusztítani a baktériumokat, de ezenfelül fizikailag is megakadályozzák terjedésüket. Szisztémás szepszis esetén a NET-ek a véráramban is létrejöhetnek.[18] Megfigyelték hogy elősegítik a véralvadást is.[19][20][21]
Patológiájuk
[szerkesztés]A normálisnál alacsonyabb neutrofilszámot neutropéniának hívják. A hiány kialakulhat a magzati fejlődés során vagy később is, mint pl. aplasztikus anémia vagy bizonyos típusú leukémia esetében. Gyógyszeres terápia (például kemoterápia) mellékhatásaként is felléphet. Az alacsony neutrofilszám jelentősen csökkenti a szervezet védekezőképességét a patogénekkel szemben.
Neutropéniáról 1500/mikroliter alatti sejtszám esetén beszélünk, 500/μl alatt pedig súlyos neutropéniáról.[22]
Alfa 1-antitripszin hiánya esetén a neutrofilek által kibocsátott elasztáz enzim nem inaktiválódik megfelelően, így gyulladáskor a szokásosnál nagyobb szövetkárosodás lép fel; ez például tüdőtágulathoz vezethet.
Az öröklődő mediterrán láz esetében egy főleg neutrofil granulocitákban kifejeződő gén (pyrin vagy marenosztrin) mutációja lép fel, ami a neutrofilek állandó aktivációja miatti lázrohamokkal, ízületi fájdalommal, hashártyagyulladással és végül amiloidózissal jár.[23]
A neutrofilek működésének zavara (a mieloperoxidáz enzim hiánya vagy csökkent granulumszám) összekapcsolható a magas vércukorszinttel.[24]
Jegyzetek
[szerkesztés]- ↑ (2000) „Neutrophils: molecules, functions and pathophysiological aspects”. Lab Invest 80 (5), 617–53. o. DOI:10.1038/labinvest.3780067. PMID 10830774.
- ↑ Klebanoff, SJ (1978). „The Neutrophil: Function and Clinical Disorders”, Kiadó: Elsevier/North-Holland Amsterdam.
- ↑ (2006. március 1.) „Neutrophils and immunity: challenges and opportunities”. Nature Reviews Immunology 6 (March), 173–82. o. DOI:10.1038/nri1785. ISSN 1474-1733. PMID 16498448.
- ↑ Jacobs, L (2010. október 1.). „Subclinical responses in healthy cyclists briefly exposed to traffic-related air pollution”. Environmental Health 9 (64), 64. o. DOI:10.1186/1476-069X-9-64. PMID 20973949. PMC 2984475.
- ↑ Waugh, DJ (2008. november 1.). „The interleukin-8 pathway in cancer”. Clinical Cancer Research 14 (21), 6735–41. o. DOI:10.1158/1078-0432.CCR-07-4843. ISSN 1078-0432. PMID 18980965.
- ↑ De Larco, JE (2004. augusztus 1.). „The Potential Role of Neutrophils in Promoting the Metastatic Phenotype of Tumors Releasing Interleukin-8”. Clinical Cancer Research 10 (15), 4895–900. o. DOI:10.1158/1078-0432.CCR-03-0760. ISSN 1078-0432. PMID 15297389.
- ↑ (2011. november 20.) „Lyn is a redox sensor that mediates leukocyte wound attraction in vivo.”. Nature 480 (7375), 109-12. o. PMID 22101434.
- ↑ (2015) „Trace element landscape of resting and activated human neutrophils on sub-micrometer level”. Metallomics 7 (6), 996–1010. o. DOI:10.1039/c4mt00346b. PMID 25832493.
- ↑ a b c d Neutrophils, Atlas of Blood Cells: Function and Pathology, 2nd, Philadelphia: Lea & Ferbiger (1988. november 4.). ISBN 0-8121-1094-3
- ↑ a b Edwards, Steven W.. Biochemistry and physiology of the neutrophil. Cambridge University Press, 6. o. (1994. november 4.). ISBN 0-521-41698-1
- ↑ (2013) „What's your age again? Determination of human neutrophil half-lives revisited”. Journal of Leukocyte Biology 94 (4), 595–601. o. DOI:10.1189/jlb.1112571. PMID 23625199.
- ↑ a b Wheater's basic histopathology: a colour atlas and text [archivált változat] (PDF), Edinburgh: Churchill Livingstone (2002. november 4.). ISBN 0-443-07001-6. Hozzáférés ideje: 2017. február 9. [archiválás ideje: 2011. november 22.]
- ↑ (2008. november 4.) „Cytokine generation, promoter activation, and oxidant-independent NF-kappaB activation in a transfectable human neutrophilic cellular model”. BMC Immunol. 9, 14. o. DOI:10.1186/1471-2172-9-14. PMID 18405381. PMC 2322942.
- ↑ (2009. november 4.) „Intravascular immunity: the host–pathogen encounter in blood vessels”. Nature Reviews Immunology 9 (5), 364–75. o, Kiadó: Nature Publishing Group. DOI:10.1038/nri2532. PMID 19390567.
- ↑ (1984. november 4.) „Localization of histaminase to the specific granule of the human neutrophil”. Immunology 52 (4), 649–58. o. PMID 6430792. PMC 1454675.
- ↑ (2004. március 5.) „Neutrophil Extracellular Traps Kill Bacteria”. Science 303 (5663), 1532–1535. o, Kiadó: AAAS. DOI:10.1126/science.1092385. ISSN 0036-8075. PMID 15001782. (Hozzáférés: 2007. április 9.)
- ↑ (2009) „Neutrophil extracellular traps contain calprotectin, a cytosolic protein complex involved in host defense against Candida albicans”. PLOS Pathogens 5 (10), e1000639. o. DOI:10.1371/journal.ppat.1000639. PMID 19876394. PMC 2763347.
- ↑ (2007. április 1.) „Platelet Toll-Like Receptor-4 Activates Neutrophil Extracellular Traps to Ensnare Bacteria in Endotoxemic and Septic Blood”. Nature Medicine 13 (4), 463–9. o, Kiadó: Nature Publishing Group. DOI:10.1038/nm1565. ISSN 1078-8956. PMID 17384648.
- ↑ (2010. szeptember 7.) „Extracellular DNA traps promote thrombosis”. Proceedings of the National Academy of Sciences of the United States of America 107 (36), 15880–5. o. DOI:10.1073/pnas.1005743107. PMID 20798043. PMC 2936604.
- ↑ (2011. november 1.) „Neutrophil Extracellular Traps Promote Deep Vein Thrombosis in Mice”. Journal of thrombosis and haemostasis : JTH 10 (1), 136–44. o. DOI:10.1111/j.1538-7836.2011.04544.x. PMID 22044575. PMC 3319651.
- ↑ (2011. szeptember 1.) „From neutrophil extracellular traps release to thrombosis: an overshooting host-defense mechanism?”. Journal of thrombosis and haemostasis : JTH 9 (9), 1791–4. o. DOI:10.1111/j.1538-7836.2011.04425.x. PMID 21718435.
- ↑ (2007;16(5):344-7.) „The diagnostic value of absolute neutrophil count, band count and morphologic changes of neutrophils in predicting bacterial infections.”. Med Princ Pract. 16 (5), 344–7. o. DOI:10.1159/000104806. PMID 17709921.
- ↑ (2004. július 1.) „Familial mediterranean fever: revisiting an ancient disease”. European Journal of Pediatrics 162 (7–8), 449–54. o. [2019. szeptember 12-i dátummal az eredetiből archiválva]. DOI:10.1007/s00431-003-1223-x. ISSN 0340-6199. PMID 12751000. (Hozzáférés: 2017. február 9.)
- ↑ (2014. május 8.) „Stress Hyperglycemia, Insulin Treatment, and Innate Immune Cells”. International Journal of Endocrinology 2014, 9. o. DOI:10.1155/2014/486403. (Hozzáférés: 2016. január 19.)
Fordítás
[szerkesztés]- Ez a szócikk részben vagy egészben a Neutrophil című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
