Indén
| Indén | |||
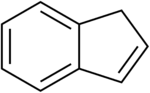 Az indén szerkezeti képlete | |||
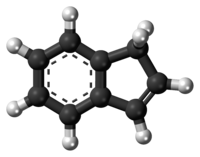
| |||
| IUPAC-név | 1H-Indén | ||
| Szabályos név | biciklo[4.3.0]nona-1,3,5,7-tetraén | ||
| Más nevek | benzociklopentadién indonaftén | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 95-13-6 | ||
| PubChem | 7219 | ||
| ChemSpider | 6949 | ||
| DrugBank | DB02815 | ||
| KEGG | C11565 | ||
| ChEBI | 41921 | ||
| |||
| |||
| InChIKey | YBYIRNPNPLQARY-UHFFFAOYSA-N | ||
| Beilstein | 635873 | ||
| Gmelin | 27265 | ||
| ChEMBL | 192812 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C9H8 | ||
| Moláris tömeg | 116,16 | ||
| Megjelenés | színtelen folyadék[1] | ||
| Sűrűség | 0,997 g/ml | ||
| Olvadáspont | −1,8 °C | ||
| Forráspont | 181,6 °C | ||
| Oldhatóság (vízben) | oldhatatlan | ||
| Savasság (pKa) | 20,1 (DMSO-ban)[2] | ||
| Mágneses szuszceptibilitás | −80,89·10−6 cm3/mol | ||
| Veszélyek | |||
| Főbb veszélyek | gyúlékony | ||
| PEL | nincs[1] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Az indén gyúlékony policiklusos szénhidrogén, képlete C9H8. Molekuláját kondenzált benzol- és ciklopenténgyűrű alkotja. Színtelen, aromás folyadék, a technikai tisztaságú anyag gyakran halványsárga színű. Fő ipari felhasználása az indén/kumaron hőre lágyuló műanyagok gyártása. A szubsztituált indének[3] és ezek indán rokonvegyületei fontos szerkezeti egységek, melyek számos természetes anyag és biológiailag aktív molekula, például a szulindak szerkezetében előfordulnak.
Kinyerése
[szerkesztés]A természetben a kőszénkátrány 175–185 °C körüli hőmérsékleten forró frakciójában fordul elő. Ebből a frakcióból – nátriummal hevítve – „indénnátrium” szilárd csapadék formájában nyerhető ki. Ez az eljárás azt használja ki, hogy az indén gyenge sav – ezt a nátrium hatására történő, indenilszármazék keletkezésével járó deprotonálódás igazolja. Az indénnátrium ezután vízgőzdesztillációval visszaalakítható indénné.[4]
Reakciói
[szerkesztés]Készségesen polimerizálódik. Savas dikromáttal oxidálva homoftálsav (o-karboxilfenilecetsav) keletkezik belőle. Dietil-oxaláttal nátrium-etoxid jelenlétében kondenzációs reakcióba lép, ekkor indén-oxálészter keletkezik, míg aldehidekkel és ketonokkal lúg jelenlétében – erősen színes – benzofulvéneket képez. Lítiumorganikus reagensekkel történő kezelés hatására indenillítium vegyületek keletkeznek:
- C9H8 + RLi → LiC9H7 + RH
Az indenil ligandum a fémorganikus kémiában, számos átmenetifém képez indenilkomplexet.
Jegyzetek
[szerkesztés]- ↑ a b c d NIOSH Pocket Guide to Chemical Hazards #0340. National Institute for Occupational Safety and Health (NIOSH)
- ↑ Bordwell FG (1988). „Equilibrium acidities in dimethyl sulfoxide solution”. Accounts of Chemical Research 21 (12), 456–463. o. DOI:10.1021/ar00156a004. Bordwell pKa Table in DMSO Archiválva 2008. október 9-i dátummal a Wayback Machine-ben.
- ↑ Das, Braja Gopal (2016. július 20.). „CoIII–Carbene Radical Approach to Substituted 1H-Indenes”. Journal of the American Chemical Society 138 (28), 8968–8975. o. DOI:10.1021/jacs.6b05434. ISSN 0002-7863.
- ↑ Gerd Collin, Rolf Mildenberg, Mechthild Zander, Hartmut Höke, William McKillip, Werner Freitag, Wolfgang Imöhl “Resins, Synthetic” Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, Weinheim, 2000.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben az Indene című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
További olvasnivalók
[szerkesztés]- W. v. Miller, Rohde (1890). „Zur Synthese von Indenderivaten”. Berichte der Deutschen Chemischen Gesellschaft 23 (2), 1881–1886. o. DOI:10.1002/cber.18900230227.
- W. v. Miller, Rohde (1890). „Zur Synthese von Indenderivaten”. Berichte der Deutschen Chemischen Gesellschaft 23 (2), 1887–1902. o. DOI:10.1002/cber.18900230228.
- Finar, I. L.. Organic Chemistry. Longman Scientific & Technical (1985). ISBN 0-582-44257-5
