Fluorbenzol
| Fluorbenzol | |||
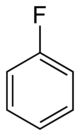 A fluorbenzol szerkezete |
 A fluorbenzol kalotta-modellje | ||
| IUPAC-név | Fluorbenzol | ||
| Más nevek | Fenil-fluorid Monofluorbenzol | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 462-06-6 | ||
| PubChem | 10008 | ||
| ChemSpider | 9614 | ||
| KEGG | C11272 | ||
| ChEBI | 5115 | ||
| |||
| |||
| InChIKey | PYLWMHQQBFSUBP-UHFFFAOYSA-N | ||
| ChEMBL | 16070 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C6H5F | ||
| Moláris tömeg | 96.103 | ||
| Megjelenés | színtelen folyadék | ||
| Sűrűség | 1,025 g/ml, folyadék | ||
| Olvadáspont | −44 °C | ||
| Forráspont | 84–85 °C | ||
| Oldhatóság (vízben) | kevéssé oldódik | ||
| Kristályszerkezet | |||
| Molekulaforma | síkalkatú | ||
| Veszélyek | |||
| NFPA 704 | |||
| R mondatok | R36, R37, R38 | ||
| S mondatok | S16, S26, S36 | ||
| Rokon vegyületek | |||
| Rokon benzol halogenidek | Klórbenzol Brómbenzol Jódbenzol | ||
| Rokon vegyületek | Benzol 1,2-Difluorbenzol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A fluorbenzol szerves vegyület, képlete C6H5F, gyakori rövidítéssel PhF. A benzol halogénezett származéka, melyben a benzolgyűrűhöz egy hidrogénatom helyett fluoratom kapcsolódik. Olvadáspontja (−44 °C) a benzolénál alacsonyabb, ami jól mutatja a szerves vegyületekbe épülő fluoratom intermolekuláris kölcsönhatásokra kifejtett jelentős hatását. A PhF és a benzol forráspontja ugyanakkor csak 4 °C-kal tér el egymástól.
Előállítása
[szerkesztés]Laboratóriumban a PhF kényelmesen előállítható a benzoldiazónium-tetrafluoroborát hőbontásával[1]
Az eljárás során a szilárd [PhN2]BF4 lánggal történő melegítésével indítják be az exoterm reakciót, melynek két illékony terméke – PhF and BF3 – könnyen elválasztható egymástól a forráspontkülönbségük alapján.
A PhF előállításáról elsőként Otto Wallach számolt be a bonni egyetemen 1886-ban. A vegyületet – a fentihez hasonlóan – szintén fenildiazónium sóból kiindulva, két lépésben állította elő. A diazónium-kloridot először piperidinidjévé alakította, melyet utána hidrogén-fluoriddal bontott el.
- [PhN2]Cl + 2 C5H10NH → PhN=N-NC5H10 + [C5H10NH2]Cl
- PhN=N-NC5H10 + 2 HF → PhF + N2 + [C5H10NH2]F
Egy érdekes tudománytörténeti megjegyzés: Wallach idején a fluort „Fl”-lel jelölték, ezért munkájában így szerepelt: „Fluorbenzol, C6H5Fl”.[2]
Technikai szintézise ciklopentadién és difluorkarbén reakciójával történik. Az első lépésben keletkező ciklopropán gyűrűbővülésen, majd hidrogén-fluorid elimináción megy keresztül.
Reakciói
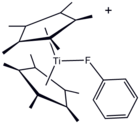
[szerkesztés]A PhF a nagyon erős C–F kötés miatt kevéssé reakcióképes vegyület. Erősen reakcióképes anyagok oldószereként használható, de fémkomplexének kristályait is előállították.[3]
A fluorbenzol fluorozásának fő terméke az 1,2-difluorbenzol.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Fluorobenzene című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Jegyzetek
[szerkesztés]- ↑ Flood, D. T. (1943). „Fluorobenzene”. Org. Synth..; Coll. Vol. 2: 295.
- ↑ Wallach, O. “Über einen Weg zur leichten Gewinnung organischer Fluorverbindungen” (Concerning a method for easily preparing organic fluorine compounds) Justus Liebig's Annalen der Chemie, 1886, Volume 235, p. 255–271; doi:10.1002/jlac.18862350303
- ↑ R.N. Perutz and T. Braun “Transition Metal-mediated C–F Bond Activation” Comprehensive Organometallic Chemistry III, 2007, Volume 1, p. 725–758; doi:10.1016/B0-08-045047-4/00028-5.