Benzonitril
| Benzonitril | |||
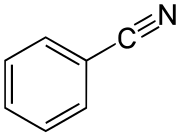 szerkezeti képlet | |||
 pálcika-modell | |||
| IUPAC-név | benzonitril | ||
| Más nevek | cianobenzol fenil-cianid | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 100-47-0 | ||
| PubChem | 7505 | ||
| RTECS szám | DI2450000 | ||
| |||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C7H5N | ||
| Moláris tömeg | 103,04 g/mol | ||
| Sűrűség | 1,0 g/ml | ||
| Olvadáspont | −13 °C | ||
| Forráspont | 188–91 °C | ||
| Oldhatóság (vízben) | <0,5 g/100 ml (22 °C) | ||
| Törésmutató (nD) | 1,5280 | ||
| Gőznyomás | 0,72 mbar (20 °C) 4,8 mbar (50 °C)[1] | ||
| Veszélyek | |||
| EU osztályozás | Ártalmas (Xn)[1] | ||
| EU Index | 608-012-00-3 | ||
| NFPA 704 | |||
| R mondatok | R21/22[1] | ||
| S mondatok | (S2), S23[1] | ||
| Lobbanáspont | 75 °C | ||
| Öngyulladási hőmérséklet | 550 °C | ||
| Robbanási határ | 1,4–7,2% | ||
| LD50 | 971 mg/kg (egér, szájon át) 720 mg/kg (patkány, szájon át)[2] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A benzonitril aromás szerves vegyület, képlete C6H5CN, rövidítve PhCN. Színtelen, mandulaszagú folyadék. Benzamid dehidratálásával vagy brómbenzol és nátrium-cianid reakciójával állítható elő.
Felhasználása
[szerkesztés]A benzonitril jól használható oldószer, és számos származék előanyaga. Aminokkal reagáltatva hidrolízist követően N-szubsztituált benzamidok állíthatók elő.[3]
A benzonitrilből fenil-magnézium-bromiddal történő reakció, majd azt követő metanolízis során Ph2C=NH (fp. 151 °C, 8 Hgmm) keletkezik.[4]
A benzonitril késői átmenetifémekkel koordinációs komplexeket képezhet, melyek szerves oldószerben oldódnak, és megfelelően labilisak, ilyen például a PdCl2(PhCN)2. A benzonitril ligandumot erősebb ligandumok könnyen kiszorítják, ezért e benzonitril komplexei hasznos szintetikus köztitermékek.[5]
Felfedezése
[szerkesztés]A benzonitrilt 1844-ben fedezte fel Hermann Fehling az ammónium-benzoát hőbomlásának termékei között. Az anyag szerkezetét is meg tudta határozni a már ismert, ammónium-formiátból hidrogén-cianidot létrehozó reakció felhasználásával. Tőle származik a benzonitril név is, és a nitrilek is erről kapták nevüket.[6]
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Benzonitrile című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások
[szerkesztés]- ↑ a b c d A benzonitril vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2011. 02. 03. (JavaScript szükséges) (angolul)
- ↑ Benzonitril (ChemIdplus)
- ↑ Cooper, F.C.; Partridge, M. W. (1963). „N-Phenylbenzamidine”. Org. Synth..; Coll. Vol. 4: 769
- ↑ Pickard, P. L.; Tolbert, T. L. (1973). „Diphenyl Ketimine”. Org. Synth..; Coll. Vol. 5: 520
- ↑ Gordon K. Anderson, Minren Lin (1990). „Bis(Benzonitrile)Dichloro Complexes of Palladium and Platinum”. Inorganic Syntheses 28, 60–63. o. DOI:10.1002/9780470132593.ch13.
- ↑ Hermann Fehling (1844). „Ueber die Zersetzung des benzoësauren Ammoniaks durch die Wärme”. Annalen der Chemie und Pharmacie 49 (1), 91–97. o. DOI:10.1002/jlac.18440490106.

