Tropon
| Tropon[1] | |||
 A tropon szerkezete |
 A tropon kalottamodellje | ||
| Más nevek | Ciklohepta-2,4,6-triénon | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 539-80-0 | ||
| PubChem | 10881 | ||
| ChemSpider | 10419 | ||
| |||
| |||
| InChIKey | QVWDCTQRORVHHT-UHFFFAOYSA-N | ||
| UNII | CO48X7SUFH | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C7H6O | ||
| Moláris tömeg | 106,12 g/mol | ||
| Sűrűség | 1,094 g/ml | ||
| Forráspont | 113 °C | ||
| Veszélyek | |||
| Lobbanáspont | >113 °C | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A tropon (IUPAC-név: ciklohepta-2,4,6-trién-1-on) nem benzoid aromás szerves vegyület.[2] 7 szénatomos gyűrűből áll három konjugált kettős kötéssel és ketocsoporttal. A hasonló tropolon (2-hidroxiciklohepta-2,4,6-trién-1-on) további alkohol (vagy enol) csoporttal rendelkezik a keton mellett. A troponok ritkák a természetes környezetben, kivéve a 2-hidroxiszármazékokat, a tropolonokat.
A tropon 1951 óta ismert, és nevezik cikloheptatrienílium-oxidnak is. A tropolon nevet M. J. S. Dewar alkotta 1945-ben az érzékelt aromásság miatt.[3]
Jellemzők
[szerkesztés]Dewar 1945-ben feltételezte, hogy a troponok aromásak lehetnek. A karbonilcsoport a triéngyűrű révén jobban polarizált, részleges pozitív töltést adva a szénatomnak és részleges negatívat az oxigénnek (A). Szélsőséges esetben a szén töltése teljes (B), tropíliumiont adva, mely aromás 6 elektronos rendszer (C).
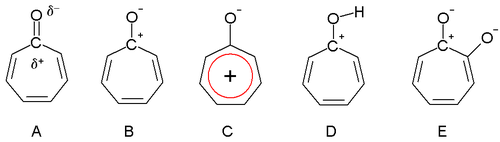
A troponok bázikusak (D) is lehetnek az aromás stabilizáció révén. Ez a savakkal való könnyű sóképződésben is megjelenik. A tropon dipólusmomentuma 4,17 D, szemben a cikloheptanon 3,04 D-ével. A különbség a dipoláris rezonanciaszerkezet stabilizációjával konzisztens.
Szintézis
[szerkesztés]Számos mód van troponok és troponszármazékok szintézisére. Két gyakori módszer erre a cikloheptatrién szelén-dioxidos oxidációja[4] és a tropinonból Hofmann-eliminációval és brómozással közvetve történő út.[2]
A tropon előállítható továbbá brómbenzolból diazometánnal UV-fényben. Ez brómtropilidént ad, ami brómozással és hidrogén-bromid-eliminációval brómtropílium-bromidot ad, melynek hidrolízisekor tropon keletkezik.[5]

Reakciók
[szerkesztés]Magas hőmérsékleten kálium-hidroxidban a tropon gyűrűszűkülésen megy át benzoesavat adva. Sok származék szintén a megfelelő arénné szűkül.[2] A tropon elektrofil szubsztitúcióban reagál például brómmal, de ez az 1,2-addíciós terméken megy keresztül, és nem aromás elektrofil szubsztitúció.[2]

A troponszármazékok a nukleofil aromás szubsztitúcióhoz hasonló nukleofil szubsztitúcióban is reagálnak.[2]
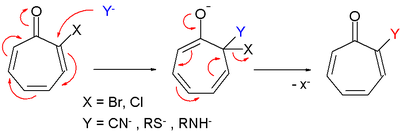
A tropon [8+3]annuláción megy át fahéjaldehiddel.[6]

Diénkarakter
[szerkesztés]A tropon diénként működik Diels–Alder-reakciókban például maleinsav-anhidriddel.[2] Vas-trikarbonillal a (butadién)vas-trikarbonilhoz hasonló adduktumokat képez.[7]
Származékok
[szerkesztés]| Név | Szerkezet | Természetes források |
|---|---|---|
| Tropolon |  |
Pseudomonas lindbergii, Pseudomonas plantarii[8] |
| Hinokitiol |  |
Cupressaceae-fák[9] |
| Stipitatinsav |  |
Talaromyces stipitatus[10] |
| Tropoditietinsav |  |
Phaeobacter piscinae, Phaeobacter inhibens, Phaeobacter gallaeciensis[11][12] |
| Kolchicin |  |
Colchicum autumnale, Gloriosa superba[13] |
További troponszármazékok például a puberulon- és puberulinsav, a rozeobakticidek, a pernambukon, a krototropon és az orobanon.[14][15][16][17][18]
Jegyzetek
[szerkesztés]- ↑ Tropone a Sigma-Aldrichon
- ↑ a b c d e f Pauson, Peter L. (1955). „Tropones and Tropolones”. Chem. Rev. 55 (1), 9–136. o. DOI:10.1021/cr50001a002.
- ↑ M. J. S. Dewar (1945). „Structure of Stipitatic Acid”. Nature 155 (3924), 50–51. o. DOI:10.1038/155050b0.
- ↑ (1993) „Inverse Electron-Demand Diels-Alder Cycloaddition of a Ketene Dithioacetal. Copper Hydride-Promoted Reduction of a Conjugated Enone. 9-Dithiolanobicyclo[3.2.2non-6-en-2-one]”. Org. Synth. 71, 181. o. DOI:10.15227/orgsyn.071.0181.
- ↑ Hans Beyer, Wolfgang Walter. Lehrbuch der Organischen Chemie. Stuttgart: S. Hirzel, 616–617. o. (1984). ISBN 3-7776-0406-2
- ↑ Vijay Nair, Manojkumar Poonoth, Sreekumar Vellalath, Eringathodi Suresh, and Rajasekaran Thirumalai (2006). „An N-Heterocyclic Carbene-Catalyzed [8 + 3] Annulation of Tropone and Enals via Homoenolate”. J. Org. Chem. 71 (23), 8964–8965; (megjegyzés). o. DOI:10.1021/jo0615706.
- ↑ (1964) „The Crystal and Molecular Structure of Tropone Iron Tricarbonyl”. Journal of the American Chemical Society 86 (24), 5429–5431. o. DOI:10.1021/ja01078a013.
- ↑ (2014. december 1.) „Synthesis of naturally occurring tropones and tropolones”. Tetrahedron 70 (49), 9281–9305. o. DOI:10.1016/j.tet.2014.07.065. PMID 25400298. PMC 4228802.
- ↑ (2014. szeptember 10.) „The Biological Activities of Troponoids and Their Use in Agriculture A Review”. Journal of Horticultural Research 22 (1), 5–19. o. DOI:10.2478/johr-2014-0001.
- ↑ (2012. május 15.) „Genetic, molecular, and biochemical basis of fungal tropolone biosynthesis”. Proceedings of the National Academy of Sciences 109 (20), 7642–7647. o. DOI:10.1073/pnas.1201469109. PMID 22508998. PMC 3356636.
- ↑ (2014. augusztus 6.) „Synthesis and bioactivity of analogues of the marine antibiotic tropodithietic acid”. Beilstein Journal of Organic Chemistry 10, 1796–1801. o. DOI:10.3762/bjoc.10.188. PMID 25161739. PMC 4142847.
- ↑ (2017. december 1.) „Dual function of tropodithietic acid as antibiotic and signaling molecule in global gene regulation of the probiotic bacterium Phaeobacter inhibens”. Scientific Reports 7 (1), 730. o. DOI:10.1038/s41598-017-00784-7. PMID 28389641. PMC 5429656.
- ↑ (2009) „GOUT”. Pharmacology and Therapeutics, 1039–1046. o. DOI:10.1016/B978-1-4160-3291-5.50079-2.
- ↑ (2009. december 10.) „Identification and biosynthesis of tropone derivatives and sulfur volatiles produced by bacteria of the marine Roseobacter clade”. Organic & Biomolecular Chemistry 8 (1), 234–246. o. DOI:10.1039/B909133E. PMID 20024154.
- ↑ (2020. szeptember 1.) „Bacterial Tropone Natural Products and Derivatives: Overview of their Biosynthesis, Bioactivities, Ecological Role and Biotechnological Potential”. ChemBioChem 21 (17), 2384–2407. o. DOI:10.1002/cbic.201900786. PMID 32239689. PMC 7497051.
- ↑ (2009. május 1.) „Pernambucone, a new tropone derivative from Croton argyroglossum”. Die Pharmazie 64 (5), 350–351. o. DOI:10.1691/ph.2009.7592. PMID 19530449.
- ↑ (2008. április 1.) „Crototropone, a new tropone derivative from Croton zehntneri”. Fitoterapia 79 (3), 236–237. o. DOI:10.1016/j.fitote.2007.12.001. PMID 18321658.
- ↑ (1981. január 1.) „A tropone derivative from orobanche rapum-genistae”. Phytochemistry 20 (4), 777–779. o. DOI:10.1016/0031-9422(81)85173-4.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Tropone című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
