N-klórszukcinimid
Megjelenés
| N-klórszukcinimid[1] | |||
 |
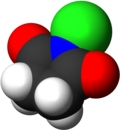
| ||
| IUPAC-név | 1-klórpirrolidin-2,5-dion | ||
| Más nevek | klórszukcinimid | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| Rövidítés | NCS | ||
| CAS-szám | 128-09-6 | ||
| PubChem | 31398 | ||
| EINECS-szám | 204-878-8 | ||
| |||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C4H4ClNO2 | ||
| Moláris tömeg | 133,53 g/mol | ||
| Megjelenés | szilárd anyag | ||
| Olvadáspont | 148–150 °C | ||
| Veszélyek | |||
| EU osztályozás | korrozív (C) | ||
| R mondatok | R22 R34 | ||
| S mondatok | S26 S36/37/39 S45 | ||
| Rokon vegyületek | |||
| Rokon imidek | szukcinimid N-brómszukcinimid | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Az N-klórszukcinimidet klórozásra[2] és enyhe oxidálószerként használják.[3]
A jód analóg N-jódszukcinimidet (NIS), és bróm analóg N-brómszukcinimidet (NBS) is hasonló célokra alkalmazzák.[4][5]
Másik rövidítése az NCLS. Oximok halogénezésére használják.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben az N-Chlorosuccinimide című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások
[szerkesztés]- ↑ N-Chlorosuccinimide a Sigma-Aldrich oldalán
- ↑ Delaney, Paul A., R. Johnstone (1985). „Solvent effects in the chlorination of tetrahydrothiophens with N-chlorosuccinimide”. Tetrahedron 41 (18), 3845–3851. o. DOI:10.1016/S0040-4020(01)91405-X.
- ↑ Kim, Kwan Soo, I. Cho, B. Yoo, Y. Song and C. Hahn (1984). „Selective oxidation of primary and secondary alcohols using di-isopropyl sulphide–N-chlorosuccinimide”. J. Chem. Soc., Chem. Commun., 762–763. o. DOI:10.1039/C39840000762.
- ↑ Beebe, T. R., R. L. Adkins, C. C. Bogardus, B. Champney, P. S. Hii, P. Reinking, J. Shadday, W. D. Weatherford, M. W. Webb, and S. W. Yates (1983). „Primary alcohol oxidation with N-iodosuccinimide”. J. Org. Chem. 48, 3126–3128. o. DOI:10.1021/jo00166a046.
- ↑ Castanet, Anne-Sophie, F. Colobert, P. Broutin (2002). „Mild and regioselective iodination of electron-rich aromatics with N-iodosuccinimide and catalytic trifluoroacetic acid”. Tetrahedron Lett. 43, 5047–5048. o. DOI:10.1016/S0040-4039(02)01010-9.
Külső hivatkozások
[szerkesztés]- N-Chlorosuccinimide és N-Iodosuccinimide az Organic Chemistry Portal lapon (angolul)
- felhasználása (angolul)
