Tapinarof
| |||
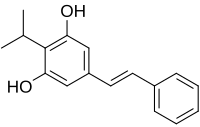
| Tapinarof | |||
| IUPAC-név | |||
| 5-[(E)-2-Phenylethen-1-yl]-2-(propan-2-yl)benzene-1,3-diol | |||
| Más nevek | Benvitimod; GSK-2894512; (E)-3,5-Dihydroxy-4-isopropyl-trans-stilbene; 3,5-Dihydroxy-4-isopropylstilbene | ||
| Kémiai azonosítók | |||
| CAS-szám | 79338-84-4 | ||
| PubChem | 6439522 | ||
| ChemSpider | 4943924 | ||
| DrugBank | DB06083 | ||
| KEGG | D11365 | ||
| |||
| InChIKey | ZISJNXNHJRQYJO-CMDGGOBGSA-N | ||
| UNII | 84HW7D0V04 | ||
| ChEMBL | 259571 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C17H18O2 | ||
| Moláris tömeg | 254,32 g/mol | ||
| Terápiás előírások | |||
| Jogi státusz | Rx-only (US) | ||
| Alkalmazás | Topikális | ||
A tapinarof (vagy benvitimod) a Vtama néven forgalmazott gyógyszer hatóanyaga.
A készítményt a plakkos pikkelysömör (psoriasis vulgaris) felületi kezelésére engedélyezték az Amerikai Egyesült Államokban (2022 május).[2][3][4][5] Az FDA a tapinarofot új farmakoterápiás csoport első vegyületeként tartja számon. Az antibiotikus hatású hatóanyag természetes eredetű vegyület, amelyet a fonalféreggel szimbiózisban élő baktérium termel.[6][7] A hatóanyag az aromás szénhidrogén-receptoron fejti ki hatását.[2][8] A Vtama lett az első számú készítmény a plakkos pikkelysömör kezelésében az Amerikai Egyesült Államokban (2022. július 15.).[9]
Gyógyászati alkalmazása
[szerkesztés]A tapinaroft felnőttek enyhe, mérsékelt és súlyos plakkos pikkelysömörének kezelésére engedélyezték.[2] A készítmény (Vtama) fázis III-as klinikai vizsgálatban hatásosnak bizonyult az atópiás dermatitisz kezelésében.[10]
Mellékhatásai
[szerkesztés]A rövid távú használat során előforduló leggyakoribb mellékhatások: szőrtüszőgyulladás, kontakt dermatitisz, fejfájás, viszketés és felső légúti fertőzés.[8][11]
Farmakológia
[szerkesztés]Hatásmechanizmus
[szerkesztés]A tapinarof az aromás szénhidrogén-receptor agonistája; gátolja a gyulladásos citokineket, modulálja a bőr védőréteg fehérjeexpresszióját, csökkenti az oxidatív stresszt és szabályozza az immunsejtek génexpresszióját.[8][12][13]
Hatásossága
[szerkesztés]Az 1%-os tapinarof krém napi egyszer alkalmazva hatásosabbnak bizonyult a vivőanyagos kontrollhoz képest; a készítmény a 12 hetes kezelés során szignifikánsan csökkentette a tüneteket.[8][14]
Elnevezése
[szerkesztés]A hatóanyag nemzetközi gyógyszerszabadneve (INN) a tapinarof.[15]
Természetes előfordulása
[szerkesztés]A tapinarof egy stilbenoid, amelyet a (Heterorhabditis nemzetségbe tartozó) fonalférgekkel szimbiózisban élő (Photorhabdus nemzetségbe tartozó) baktériumok termelnek. A tapinarof a stilbenoid bioszintézis alternatív, ketoszintáz katalizálta útvonalán keletkezik két β-ketoacil-tioészter kondenzcióján keresztül. A hatóanyagot a rovarpatogén (entomopatogén) Heterorhabditis megidis fonalféreggel szimbiózisban élő baktérium termeli.[6] A Galleria mellonella, a nagy viaszmoly fertőzött lárváival végzett kísérletek alátámasztják azt a hipotézist, hogy a vegyület antibakteriális hatású, megakadályozza a fonálféreggel fertőzött rovartetem rothadását.[7]

Jegyzetek
[szerkesztés]- ↑ Vtama- tapinarof cream. DailyMed , 2022. május 23. [2022. július 3-i dátummal az eredetiből archiválva]. (Hozzáférés: 2022. június 19.)
- ↑ a b c DailyMed - VTAMA- tapinarof cream. dailymed.nlm.nih.gov. (Hozzáférés: 2023. június 19.)
- ↑ Drugs@FDA: FDA-Approved Drugs (angol nyelven). www.accessdata.fda.gov. (Hozzáférés: 2023. június 19.)
- ↑ https://www.facebook.com/Drugscom:+Vtama (tapinarof) FDA Approval History (angol nyelven). Drugs.com. (Hozzáférés: 2023. június 19.)
- ↑ Dermavant Sciences (amerikai angol nyelven). (Hozzáférés: 2023. június 19.)
- ↑ a b Joyce, Susan A., Itamar (2008. február 22.). „Bacterial Biosynthesis of a Multipotent Stilbene” (angol nyelven). Angewandte Chemie International Edition 47 (10), 1942–1945. o. DOI:10.1002/anie.200705148.
- ↑ a b Hu, Kaiji (2000. augusztus 1.). „Antibiotic production in relation to bacterial growth and nematode development in Photorhabdus–Heterorhabditis infected Galleria mellonella larvae” (angol nyelven). FEMS Microbiology Letters 189 (2), 219–223. o. DOI:10.1111/j.1574-6968.2000.tb09234.x.
- ↑ a b c d Bissonnette, Robert, David S. (2021. április 1.). „Tapinarof in the treatment of psoriasis: A review of the unique mechanism of action of a novel therapeutic aryl hydrocarbon receptor–modulating agent”. Journal of the American Academy of Dermatology 84 (4), 1059–1067. o. DOI:10.1016/j.jaad.2020.10.085. ISSN 0190-9622.
- ↑ OTSZ Online - Kísérleti szer atópiás dermatitiszre. OTSZ Online. (Hozzáférés: 2023. június 19.)
- ↑ Dermavant Reports Positive Topline Results from ADORING 2 Atopic Dermatitis Phase 3 Trial of VTAMA® (tapinarof) Cream, 1% Once Daily in Adults and Children as Young as 2 Years Old (angol nyelven). www.businesswire.com, 2023. március 15. (Hozzáférés: 2023. június 19.)
- ↑ (2021. december 1.) „Phase 3 Trials of Tapinarof Cream for Plaque Psoriasis”. The New England Journal of Medicine 385 (24), 2219–2229. o. DOI:10.1056/NEJMoa2103629. PMID 34879448.
- ↑ (2019. október 1.) „Aryl Hydrocarbon Receptor in Atopic Dermatitis and Psoriasis”. International Journal of Molecular Sciences 20 (21), 5424. o. DOI:10.3390/ijms20215424. PMID 31683543.
- ↑ (2018. június 1.) „Systemic Pharmacokinetics, Safety, and Preliminary Efficacy of Topical AhR Agonist Tapinarof: Results of a Phase 1 Study”. Clinical Pharmacology in Drug Development 7 (5), 524–531. o. DOI:10.1002/cpdd.439. PMID 29389078.
- ↑ Lebwohl (2021. december 9.). „Phase 3 Trials of Tapinarof Cream for Plaque Psoriasis”. The New England Journal of Medicine 385 (24), 2219–2229. o. DOI:10.1056/NEJMoa2103629. ISSN 1533-4406. PMID 34879448.
- ↑ (2017) „International nonproprietary names for pharmaceutical substances (INN): recommended INN: list 78”. WHO Drug Information 31 (3).
Fordítás
[szerkesztés]- Ez a szócikk részben vagy egészben a Tapinarof című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
