Restrikciós endonukleáz
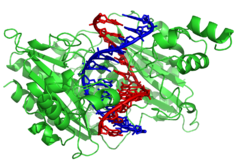
A restrikciós endonukleáz (vagy restrikciós enzim) olyan enzim, amely képes felismerni egy rövid nukleotidszekvenciát a kétszálú DNS-en belül és azon a helyen – vagy a közelében – elvágja a DNS-t.[1] Ezeket az enzimeket baktériumok és archebaktériumok termelik és a vírusfertőzés elleni védekezésben játszanak szerepet.[2] A sejten belül azokat az idegen nukleinsavakat vágják el, melyekben az általuk felismert szekvencián egy metiláz enzim korábban nem helyezett el egy metilcsoportot (és ezáltal korlátozzák, restrikció alá helyezik a vírusszaporodást). A két folyamat együtt alkotja a restrikciós modifikációs rendszert.
Eddig több mint 3000 restrikciós endonukleázt tanulmányoztak részletesen és közülük mintegy 600 kereskedelmi forgalomba is került.[3] A molekuláris biológiai laboratóriumok gyakran használják ezeket az enzimeket, többek között a klónozás és a génsebészet alapvető eszközei.
Felfedezése
[szerkesztés]Az 1950-es évek elején fedezte fel Salvador Luria és Giuseppe Bertani, hogy a λ-fág egyes Escherichia coli törzsekben jól szaporodik, míg másokban sokkal kevésbé.[4] Bizonyos törzsek képesek voltak csökkenteni a vírus fertőzőképességét, amely más törzsekbe való átvitel után is megmaradt. Az 1960-as években Werner Arber és Matthew Meselson kimutatta, hogy a restrikciós hatás a fág DNS-ének feldarabolása miatt következik be és az ezt végző enzimet restrikciós endonukláznak (a nukleinsav közepén vágó enzimnek) nevezték el.[5] Ezek az endonuklázok az I-es típushoz tartoztak, amelyek a felismerőhely közelében random módon vágják el a DNS-t. 1970-ben Hamilton O. Smith, Thomas Kelly és Kent Welcox felfedezte az első II-es típusú enzimet, a Haemophilus influenzae HindII fehérjéjét, amely a felismerőhelyen belül vágott.[6] Daniel Nathans mutatta ki, hogy a restrikciós endonukleázok specifikus darabokra vágják az SV40 (simian virus 40) DNS-ét, amiket aztán gélelektroforézissel szét lehet választani.[7] A módszerrel el lehetett kezdeni a vírusgenom feltérképezését. Werner Arber, Daniel Nathans, és Hamilton O. Smith 1978-ban orvosi Nobel-díjat kapott a restrikciós enzimekkel végzett munkájukért.
A felismerőhely
[szerkesztés]A restrikciós endonukleázok egy bizonyos rövid nukleotidmintázatot ismernek fel a DNS-en belül. A felismerőhely általában 4-8 nukleotid hosszúságú és sok esetben palindrom, vagyis a bázisok sorrendje ugyanaz előre és visszafelé olvasva is. A palindrom szakasz lehet tükörszerű, amikor ugyanazon a szálon lehet visszafelé is elolvasni a szekvenciát (például GTAATG). Gyakoribb azonban, hogy az ismétlődés megfordított, vagyis a komplementer DNS-szálon lehet olvasni fordított irányban (például GTATAC, a bázispárosodásnak megfelelően a komplementer szálon visszafelé olvasva szintén GTATAC lesz).
Egyes endonukleázok „tompa” végű fragmenteket produkálnak, mint például a SmaI:

A laboratóriumok inkább olyan enzimeket használnak amelyek „ragadós” végű darabokat produkálnak, mint az EcoRI:

Melegítés hatására a szálak szétválaszthatók és utána egy másik, ugyanilyen enzimmel elvágott DNS-el összehibridizálhatóak. Az elvágott szálak pedig a DNS-ligáz enzim segítségével összeforraszthatóak.
Azokat a restrikciós endonuklázokat, amelyeknek ugyanaz a felismerőhelyük neoskizomereknek nevezik. Azokat pedig, amelyeknek a hasítóhelyük is megegyezik, izoskizomernek.
A restrikciós endonukleázok elnevezése a következő szabály szerint áll össze: első betűje annak a baktérium genusának első betűje, amelyikből izolálták; utána a fajnév első két betűje; a törzs – ha van – első betűje, és végül egy sorszám. Az EcoRI például az Escherichia coli RY13 törzséből elsőként izolált enzim.[8]
Típusok
[szerkesztés]A baktériumokban előforduló restrikciós endonukleázokat négy csoportba (I, II III, és IV) sorolják, szerkezetük, kofaktorigényük, felismerőhelyük és hasítóhelyük alapján:[9]
- I. típus, a felismerőhelyen kívül vágja a DNS-t; működéséhez ATP-re és S-adenozil-L-metioninra van szüksége; hasító és metiláló funkcióval is rendelkezik.
- II. típus, a felismerőhelyen belül vagy hozzá nagyon közel vág; magnéziumionra van szüksége, metilázfunkcióval nem rendelkezik.
- III. típus, a felismerőhely közelében vág; szüksége van ATP-re (de nem hidrolizálja el); az S-adenozil-L-metionin stimulálja a reakciót, de nem feltétlenül szükséges; egy komplexben van a metilázzal.
- IV. típus, módosított (vagyis metilált, hidroximetilált vagy glükozil-hodroximetilált) DNS-t vág.
Mesterséges restrikciós enzimek
[szerkesztés]A természetes enzimek szerkezetének kutatása lehetővé tette mesterséges endonukleázok létrehozását. Ilyenkor egy DNS-kötő domént egy nukleázdoménnel (például a FokI hasítódoménját) kombinálnak össze.[10] Az ilyen enzimek specificitása tetszés szerint módosítható, akár 36 bázispár hosszú szekvenciát is felismerhetnek.
Felhasználás
[szerkesztés]A ragadós véget produkáló restrikciós enzimeket különböző eredetű DNS-szálak egymáshoz illesztésére lehet felhasználni, így főleg a génklónozási (nem összetévesztendő a teljes szervezet klónozásával) és génsebészeti kísérletekben. Erre a célra speciális plazmidvektorokat fejlesztettek ki, melyeken több, gyakran használt enzim felismerőhelye is megtalálható. Mind a plazmidot, mind az átviendő DNS-szakaszt restrikciós enzimmel kezelik, összekeverés után felmelegítéssel elválasztják egymástól a szálakat, majd visszahűtés után (miután a kétszálú DNS-konformáció helyreállt) ligáz enzimmel összekötik az endonukleáz által elvágott szálat.[11]
A restrikciós endonukleázok egyes pontmutációk gyors és olcsó felismerésére is alkalmasak, amennyiben a mutáció elront egy felismerőhelyet (vagy létrehozza azt). Ilyenkor az endonukleázos emésztés után az eredeti szakasz a gélelektroforézis során két rövidebb, míg a mutáns verzió egyetlen, hosszabb csíkot fog mutatni.[12]
Restrikciós endonukleázokat használnak a törvényszéki orvostan által is alkalmazott DNS-ujjlenyomat meghatározásánál is. Az egyes hasítóhelyek közötti távolság egyénenként eltérő lehet, ami két minta közötti azonosság vagy akár rokonság gyors meghatározását teszi lehetővé.
A molekuláris biológia korai időszakában, amikor még nem álltak rendelkezésre olcsó szekvenálási módszerek, a restrikciós enzimeket a kisebb (főleg vírus-) genomok feltérképezésére is használták.
Példák
[szerkesztés]Az alábbi táblázatban néhány restrikciós enzim, felismerő- és hasítóhelyük látható:[13]
| Enzim | Eredet | Felismerőhely | Hasítóhely |
|---|---|---|---|
| EcoRI | Escherichia coli |
5'GAATTC 3'CTTAAG |
5'---G AATTC---3' 3'---CTTAA G---5' |
| EcoRII | Escherichia coli |
5'CCWGG 3'GGWCC |
5'--- CCWGG---3' 3'---GGWCC ---5' |
| BamHI | Bacillus amyloliquefaciens |
5'GGATCC 3'CCTAGG |
5'---G GATCC---3' 3'---CCTAG G---5' |
| HindIII | Haemophilus influenzae |
5'AAGCTT 3'TTCGAA |
5'---A AGCTT---3' 3'---TTCGA A---5' |
| TaqI | Thermus aquaticus |
5'TCGA 3'AGCT |
5'---T CGA---3' 3'---AGC T---5' |
| NotI | Nocardia otitidis |
5'GCGGCCGC 3'CGCCGGCG |
5'---GC GGCCGC---3' 3'---CGCCGG CG---5' |
| HinfI | Haemophilus influenzae |
5'GANTCA 3'CTNAGT |
5'---G ANTC---3' 3'---CTNA G---5' |
| Sau3A | Staphylococcus aureus |
5'GATC 3'CTAG |
5'--- GATC---3' 3'---CTAG ---5' |
| PvuII* | Proteus vulgaris |
5'CAGCTG 3'GTCGAC |
5'---CAG CTG---3' 3'---GTC GAC---5' |
| SmaI* | Serratia marcescens |
5'CCCGGG 3'GGGCCC |
5'---CCC GGG---3' 3'---GGG CCC---5' |
| HaeIII* | Haemophilus aegyptius |
5'GGCC 3'CCGG |
5'---GG CC---3' 3'---CC GG---5' |
| HgaI[14] | Haemophilus gallinarum |
5'GACGC 3'CTGCG |
5'---NN NN---3' 3'---NN NN---5' |
| AluI* | Arthrobacter luteus |
5'AGCT 3'TCGA |
5'---AG CT---3' 3'---TC GA---5' |
| EcoRV* | Escherichia coli |
5'GATATC 3'CTATAG |
5'---GAT ATC---3' 3'---CTA TAG---5' |
| EcoP15I | Escherichia coli |
5'CAGCAGN25NN 3'GTCGTCN25NN |
5'---CAGCAGN25 NN---3' 3'---GTCGTCN25NN ---5' |
| KpnI[15] | Klebsiella pneumoniae |
5'GGTACC 3'CCATGG |
5'---GGTAC C---3' 3'---C CATGG---5' |
| PstI[15] | Providencia stuartii |
5'CTGCAG 3'GACGTC |
5'---CTGCA G---3' 3'---G ACGTC---5' |
| SacI[15] | Streptomyces achromogenes |
5'GAGCTC 3'CTCGAG |
5'---GAGCT C---3' 3'---C TCGAG---5' |
| SalI[15] | Streptomyces albus |
5'GTCGAC 3'CAGCTG |
5'---G TCGAC---3' 3'---CAGCT G---5' |
| ScaI*[15] | Streptomyces caespitosus |
5'AGTACT 3'TCATGA |
5'---AGT ACT---3' 3'---TCA TGA---5' |
| SpeI | Sphaerotilus natans |
5'ACTAGT 3'TGATCA |
5'---A CTAGT---3' 3'---TGATC A---5' |
| SphI[15] | Streptomyces phaeochromogenes |
5'GCATGC 3'CGTACG |
5'---GCATG C---3' 3'---C GTACG---5' |
| StuI*[16][17] | Streptomyces tubercidicus |
5'AGGCCT 3'TCCGGA |
5'---AGG CCT---3' 3'---TCC GGA---5' |
| XbaI[15] | Xanthomonas badrii |
5'TCTAGA 3'AGATCT |
5'---T CTAGA---3' 3'---AGATC T---5' |
Kódok:
* = tompa vég
N = bármilyen, C,G,T vagy A nukleotid
W = A vagy T
Jegyzetek
[szerkesztés]- ↑ Roberts RJ (November 1976). "Restriction endonucleases". CRC Crit. Rev. Biochem. 4 (2): 123–64.
- ↑ Arber W, Linn S (1969). "DNA modification and restriction". Annu. Rev. Biochem. 38: 467–500
- ↑ Roberts RJ, Vincze T, Posfai J, Macelis D. (2007). "REBASE—enzymes and genes for DNA restriction and modification". Nucleic Acids Res 35 (Database issue): D269–70.
- ↑ Luria SE, Human ML (October 1952). "A nonhereditary, host-induced variation of bacterial viruses". J. Bacteriol. 64 (4): 557–69.
- ↑ Meselson M, Yuan R (March 1968). "DNA restriction enzyme from E. coli". Nature 217 (5134): 1110–4.
- ↑ Smith HO, Wilcox KW (July 1970). "A restriction enzyme from Hemophilus influenzae. I. Purification and general properties". J. Mol. Biol. 51 (2): 379–91.
- ↑ Danna K, Nathans D (December 1971). "Specific cleavage of simian virus 40 DNA by restriction endonuclease of Hemophilus influenzae". Proc. Natl. Acad. Sci. U.S.A. 68 (12): 2913–7.
- ↑ Smith HO, Nathans D (December 1973). "Letter: A suggested nomenclature for bacterial host modification and restriction systems and their enzymes". J. Mol. Biol. 81 (3): 419–23.
- ↑ Bickle TA, Krüger DH (June 1993). "Biology of DNA restriction". Microbiol. Rev. 57 (2): 434–50.
- ↑ Kim YG, Cha J, Chandrasegaran S (February 1996). "Hybrid restriction enzymes: zinc finger fusions to Fok I cleavage domain". Proc. Natl. Acad. Sci. U.S.A. 93 (3): 1156–60.
- ↑ Geerlof A. "Cloning using restriction enzymes". European Molecular Biology Laboratory - Hamburg.
- ↑ Wolff JN, Gemmell NJ (February 2008). "Combining allele-specific fluorescent probes and restriction assay in real-time PCR to achieve SNP scoring beyond allele ratios of 1:1000". BioTechniques 44 (2): 193–4, 196, 199.
- ↑ Roberts RJ (January 1980). "Restriction and modification enzymes and their recognition sequences". Nucleic Acids Res. 8 (1): r63–r80.
- ↑ Roberts RJ (1988). „Restriction enzymes and their isoschizomers”. Nucleic Acids Res. 16 Suppl, r271–313. o. DOI:10.1093/nar/16.suppl.r271. PMID 2835753. PMC 340913.
- ↑ a b c d e f g Krieger M, Scott MP, Matsudaira PT, Lodish HF, Darnell JE, Zipursky L, Kaiser C, Berk A. Molecular Cell Biology, 5th, New York: W.H. Freeman and Company (2004). ISBN 0-7167-4366-3
- ↑ Stu I from Streptomyces tubercidicus. Sigma-Aldrich. (Hozzáférés: 2008. június 7.)
- ↑ Shimotsu H, Takahashi H, Saito H (1980. November). „A new site-specific endonuclease StuI from Streptomyces tubercidicus”. Gene 11 (3–4), 219–25. o. DOI:10.1016/0378-1119(80)90062-1. PMID 6260571.
Fordítás
[szerkesztés]- Ez a szócikk részben vagy egészben a Restriction enzyme című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
